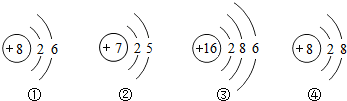题目内容
 (2013?松北区二模)化学课外小组的同学以“氢氧化钠变质程度”为课题,进行科学探究活动,请根据己学知识完成下列探究问题.
(2013?松北区二模)化学课外小组的同学以“氢氧化钠变质程度”为课题,进行科学探究活动,请根据己学知识完成下列探究问题.提出问题:氢氧化钠变质程度是怎样的?
制定计划:甲同学设计的实验如右图所示,他们在实验中都进行了规范的操作和细致的观察.
收集证据:你认为实验②中应观察到的现象是
出现白色沉淀
出现白色沉淀
;解释与结论:甲同学在实验①中,滴加几滴稀盐酸后,没有观察到明显现象,其原因是
稀盐酸不足,只能够和氢氧化钠反应
稀盐酸不足,只能够和氢氧化钠反应
;反思与交流:反思后甲同学在实验②基础上继续实验,其作法是
继续滴加氯化钡溶液,直至不再产生白色沉淀;取上层清液,加入试管中,滴加酚酞试液,酚酞试液变红色
继续滴加氯化钡溶液,直至不再产生白色沉淀;取上层清液,加入试管中,滴加酚酞试液,酚酞试液变红色
由此证明了样品中含有的物质是氢氧化钠和碳酸钠
氢氧化钠和碳酸钠
.分析:氢氧化钠能够吸收水和二氧化碳,吸收二氧化碳后,二氧化碳能和氢氧化钠反应生成碳酸钠和水,从而使氢氧化钠变质;
氯化钙溶液量多时,和氢氧化钠溶液混合可能出现氢氧化钙沉淀,所以继续实验时,改为滴加氯化钡溶液.
氯化钙溶液量多时,和氢氧化钠溶液混合可能出现氢氧化钙沉淀,所以继续实验时,改为滴加氯化钡溶液.
解答:解:收集证据:
变质的氢氧化钠中含有碳酸钠,加入氯化钙溶液时会出现白色沉淀,因为碳酸钠能和氯化钙反应生成碳酸钙沉淀和氯化钠.
故填:出现白色沉淀.
解释与结论:
甲同学在实验①中,滴加几滴稀盐酸后,没有观察到明显现象,其原因是:稀盐酸不足,只能够和氢氧化钠反应.
故填:稀盐酸不足,只能够和氢氧化钠反应.
反思与交流:
在实验②基础上继续实验,其作法是:继续滴加氯化钡溶液,直至不再产生白色沉淀;取上层清液,加入试管中,滴加酚酞试液,酚酞试液变红色,由此证明了样品中含有的物质是氢氧化钠和碳酸钠.
故填:继续滴加氯化钡溶液,直至不再产生白色沉淀;取上层清液,加入试管中,滴加酚酞试液,酚酞试液变红色;氢氧化钠和碳酸钠.
变质的氢氧化钠中含有碳酸钠,加入氯化钙溶液时会出现白色沉淀,因为碳酸钠能和氯化钙反应生成碳酸钙沉淀和氯化钠.
故填:出现白色沉淀.
解释与结论:
甲同学在实验①中,滴加几滴稀盐酸后,没有观察到明显现象,其原因是:稀盐酸不足,只能够和氢氧化钠反应.
故填:稀盐酸不足,只能够和氢氧化钠反应.
反思与交流:
在实验②基础上继续实验,其作法是:继续滴加氯化钡溶液,直至不再产生白色沉淀;取上层清液,加入试管中,滴加酚酞试液,酚酞试液变红色,由此证明了样品中含有的物质是氢氧化钠和碳酸钠.
故填:继续滴加氯化钡溶液,直至不再产生白色沉淀;取上层清液,加入试管中,滴加酚酞试液,酚酞试液变红色;氢氧化钠和碳酸钠.
点评:化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,并有助于提高观察、实验能力.所以,对化学实验不仅要认真观察,还应掌握观察实验现象的方法.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案
相关题目
 (2013?松北区二模)黑龙江网络广播电视台讯17日,正在建设中的哈齐客运专线松花江特大桥,开始铺设桥面.大桥的桥面从北岸开始向江心铺设,已经进入江中200多米.下列有关认识不正确的是( )
(2013?松北区二模)黑龙江网络广播电视台讯17日,正在建设中的哈齐客运专线松花江特大桥,开始铺设桥面.大桥的桥面从北岸开始向江心铺设,已经进入江中200多米.下列有关认识不正确的是( )