题目内容
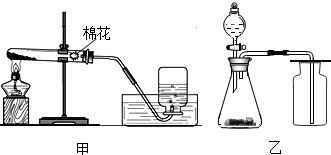
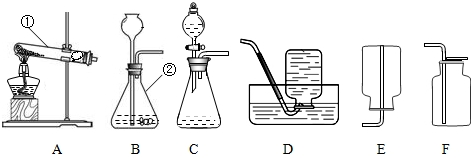
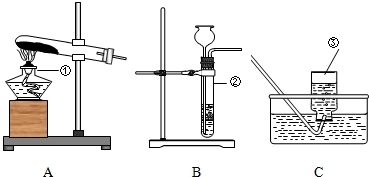
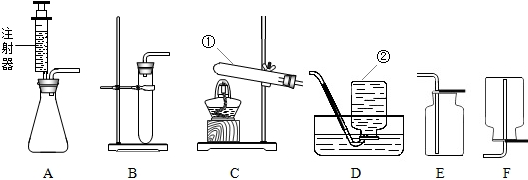
下图是实验室制取氧气的装置图.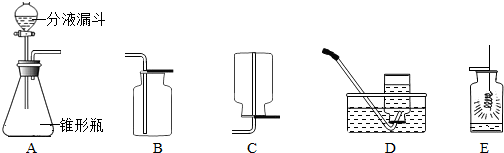
回答下列问题:
(1)分液漏斗中应放入的物质是
(2)写出该方法制取氧气的化学方程式
(3)利用E图做铁丝燃烧实验时,应注意在瓶底
(4)铁丝在空气中
分析:本题较综合地考查了氧气的制取原理、装置、收集方法,以及氧气的性质.解答时要结合所学的知识和实验经验,经认真分析后要有针对性地回答.气体制备装置的选择要考虑反应物的状态和反应条件,有固固加热型和固液常温型;选择收集气体的方法时要考虑气体在水中的溶解性和气体与空气密度的相对大小,有排水集气法和向上排空气法、向下排空气法.
解答:解:(1)A装置是固液常温型制气体装置,所以分液漏斗中应该放过氧化氢溶液,在锥形瓶里放二氧化锰,通过调节分液漏斗的阀门,即可控制滴加速度,也就能控制反应速度;
(2)过氧化氢分解后生成水和氧气,可用化学方程式表示为:2H2O2
2H2O+O2↑;由于氧气不易溶于水且密度比空气大,故可用排水法或向上排空气法收集氧气,排空气法收集的氧气往往混有较多的空气,不够纯净,故选D;
(3)铁丝在氧气中燃烧时放出的热量很多,生成物呈熔融状态,直接落到瓶底,会使瓶底破裂,因此常在实验前预先放少量的水或细沙,将铁丝绕城螺旋状,是增大铁丝与氧气的接触面积,有利于铁丝燃烧;
(4)由于空气中氧气的浓度较小,因此铁丝在空气里不能燃烧,而在氧气的集气瓶中由于氧气很纯,所以铁丝能剧烈燃烧,生成黑色的固体,是四氧化三铁,该反应可用化学方程式表示为:3Fe+2O2
Fe3O4.
故答案是:
(1)过氧化氢溶液、二氧化锰;
(2)2H2O2
2H2O+O2↑、D;
(3)留有少量的水、增大铁丝与氧气的接触面积;
(4)不能、氧气的浓度、3Fe+2O2
Fe3O4.
(2)过氧化氢分解后生成水和氧气,可用化学方程式表示为:2H2O2
| ||
(3)铁丝在氧气中燃烧时放出的热量很多,生成物呈熔融状态,直接落到瓶底,会使瓶底破裂,因此常在实验前预先放少量的水或细沙,将铁丝绕城螺旋状,是增大铁丝与氧气的接触面积,有利于铁丝燃烧;
(4)由于空气中氧气的浓度较小,因此铁丝在空气里不能燃烧,而在氧气的集气瓶中由于氧气很纯,所以铁丝能剧烈燃烧,生成黑色的固体,是四氧化三铁,该反应可用化学方程式表示为:3Fe+2O2
| ||
故答案是:
(1)过氧化氢溶液、二氧化锰;
(2)2H2O2
| ||
(3)留有少量的水、增大铁丝与氧气的接触面积;
(4)不能、氧气的浓度、3Fe+2O2
| ||
点评:本题就考查的内容来说,不算太难,但由于氧气的制取和性质是重点内容,在考试中经常出现,要引起足够地重视.

练习册系列答案
相关题目