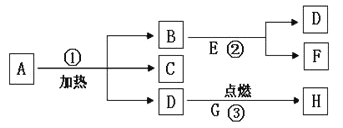
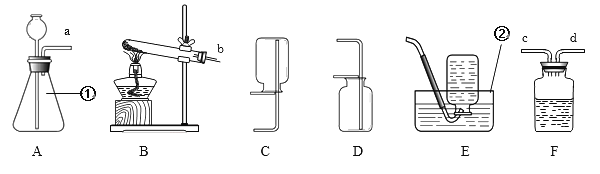
题目内容
【题目】水是生命之源,化学兴趣小组为了探究“水的净化”过程,从运河中取了水样,观察到:水样呈黄色,有异味,浑浊,有固体小颗粒。
(1)①现对水样进行过滤后向滤液中加入活性炭,利用其___________性除去水样中的颜色和异味,该过程属于________________(填“物理”或“化学”)变化。
②做好生活饮用水消毒工作,是预防肠道传染病的关键。适用于饮用水消毒的常用消毒剂有:漂白粉。漂白粉的主要成分是氯化钙【CaCl2】和次氯酸钙【Ca(ClO)2】。根据漂白粉的信息,请你判断漂白粉属于 (纯净物、混合物),关于漂白粉的说法中,合理的是:
A.氯化钙【CaCl2】和次氯酸钙【Ca(ClO)2】中氯元素的化合价相同
B.氯化钙【CaCl2】和次氯酸钙【Ca(ClO)2】都是含氧化合物
C.氯化钙【CaCl2】和次氯酸钙【Ca(ClO)2】均属于化合物
D.次氯酸钙【Ca(ClO)2】中含有原子团ClO
(2)硬水会给生产、生活带来许多不便。可以加入 来检验硬水还是软水
(3)下图表示自来水消毒过程中发生的一个反应的微观过程:
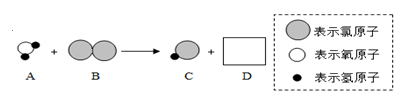
①上述物质中,B的类别是 , C的化学式是_ _ ___;
②物质D中一定含有的一种元素是 _ __。
(4)下图为电解水的实验装置图。接通电源观察两电极都有气泡产生。
①通电一段时间后,玻璃管2中收集到的气体是 (填化学式),
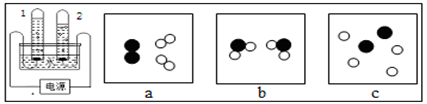
②图中a、b、c表示电解水时,反应实质的微观示意图,其正确的顺序是 。
(5)高铁酸钠(Na2FeO4)是被科学家们公认为绿色消毒剂。它的消毒和除污效果全面优于含氯消毒剂。根据获得的信息计算:
a.高铁酸钠中Na、Fe、O元素的质量比为 。
b.高铁酸钠中铁元素的质量分数为 。
c.与232g四氧化三铁含氧量相等的高铁酸钠的质量为 。
【答案】(1)①吸附,物理②混合物CD
(2)肥皂水(3)①单质,HCl;②氧元素。
(4)①收集到的气体是H2,②bca。
(5)a.23:28:32 b.33.7% c.166g
【解析】
试题分析∶由题中信息知,﹙1)①现对水样进行过滤后向滤液中加入活性炭,利用其吸附性除去水样中的颜色和异味,该过程属于物理变化。②做好生活饮用水消毒工作,是预防肠道传染病的关键。适用于饮用水消毒的常用消毒剂有:漂白粉。漂白粉的主要成分是氯化钙【CaCl2】和次氯酸钙【Ca(ClO)2】。根据漂白粉的信息,知漂白粉属于混合物,关于漂白粉的说法中,合理的是:C.氯化钙【CaCl2】和次氯酸钙【Ca(ClO)2】均属于化合物。D.次氯酸钙【Ca(ClO)2】中含有原子团ClO。(2)硬水会给生产、生活带来许多不便。可以加入肥皂水来检验硬水还是软水。(3)①上述物质中,B的类别是单质,C的化学式是HCl;②物质D中一定含有的一种元素是氧元素。(4)①通电一段时间后,玻璃管2中收集到的气体是H2,②图中a、b、c表示电解水时,反应实质的微观示意图,其正确的顺序是bca。(5)高铁酸钠(Na2FeO4)是被科学家们公认为绿色消毒剂。它的消毒和除污效果全面优于含氯消毒剂。根据获得的信息计算a.高铁酸钠中Na、Fe、O元素的质量比为2×23∶56∶16×4=23∶28∶32.b.高铁酸钠中铁元素的质量分数为56/﹙23×2+56+16×4﹚×100%=33.7%.c.与232g四氧化三铁含氧量相等的高铁酸钠的质量为232g × 56 × 3/﹙3 × 56+16 × 4﹚ × 100% = x × 56/﹙23 × 2 + 56 + 16 × 4﹚ × 100%,x=166g.
考点∶考查探究“水的净化”过程及与水相关的知识。