题目内容
(1)请写出相应的化学符号或名称
①2个汞原子______; ②氧化铝中氧元素的化合价______;
③NH4+______; ④2H2O______.
(2)请在H、O、N、S、Na等4种元素中选择恰当的元素,组成符合下列要求的物质,并将其化学式填写在相对应的位置上
①一种重要化工产品,能使湿润的红色石蕊试纸变蓝的气体是______;
②一种大气污染物,容易造成硫酸型酸雨的气体是______;
③既可作为消毒剂,也可用于实验室制取氧气的液体试剂是______;
④一种盐______.
解:(1)①2个汞原子表示为:2Hg;
②氧化铝中氧元素的化合价为: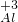 2O3;
2O3;
③NH4+表示铵根离子④2H2O表示2个水分子;
(2)①氨气溶于水显碱性,能使湿润的红色石蕊试纸变蓝;
②煤燃烧产生的二氧化硫气体容易造成硫酸型酸雨;
③双氧水能用于作消毒剂,也可用于实验室制取氧气的试剂;
④由H、O、N、S、Na这几种元素组成盐有多种,例如硫酸钠等.
故答案为:(1)①2Hg; ②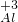 2O3;③铵根离子④2个水分子;(2)①NH3;②SO2;③;H2O2④Na2SO4.
2O3;③铵根离子④2个水分子;(2)①NH3;②SO2;③;H2O2④Na2SO4.
分析:根据要化学用语表达的对象是分子、原子、离子、还是化合价,再在相应的化学符号周围加上适当的数字和符号组成化学用语来正确地表达其意义.熟悉一些生活中常见物质的性质以及用途.
点评:本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础.书写物质的化学式时要遵循两个原则:要根据客观事实书写;不能主观臆造事实上不存在的化学式.
②氧化铝中氧元素的化合价为:
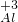 2O3;
2O3;③NH4+表示铵根离子④2H2O表示2个水分子;
(2)①氨气溶于水显碱性,能使湿润的红色石蕊试纸变蓝;
②煤燃烧产生的二氧化硫气体容易造成硫酸型酸雨;
③双氧水能用于作消毒剂,也可用于实验室制取氧气的试剂;
④由H、O、N、S、Na这几种元素组成盐有多种,例如硫酸钠等.
故答案为:(1)①2Hg; ②
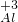 2O3;③铵根离子④2个水分子;(2)①NH3;②SO2;③;H2O2④Na2SO4.
2O3;③铵根离子④2个水分子;(2)①NH3;②SO2;③;H2O2④Na2SO4.分析:根据要化学用语表达的对象是分子、原子、离子、还是化合价,再在相应的化学符号周围加上适当的数字和符号组成化学用语来正确地表达其意义.熟悉一些生活中常见物质的性质以及用途.
点评:本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础.书写物质的化学式时要遵循两个原则:要根据客观事实书写;不能主观臆造事实上不存在的化学式.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
根据初中化学知识,探究空气中氧气含量实验.小明根据所学内容,红磷、白磷、木炭、镁条都可以和氧气发生反应,但是哪种物质更适用于测定空气中氧气含量,小明进行如下探究.
探究问题:红磷、白磷、木炭、镁条几种物质,哪种更适用于测定空气中氧气含量?
查阅资料:
①红磷、白磷对比情况
②镁条可以与空气中多种物质反应,如N2、CO2等
探究过程:如下图所示,按照实验装置进行实验,探究几种物质测定空气中O2含量的可行性.
(1)红磷、白磷探究实验
小明认为选用红磷进行实验,其原因是 .
(2)若将实验药品改为木炭,反应结束后降至室温,打开止水夹,水不倒吸入集气瓶的原因是 .
(3)若将实验药品改为镁条,反应结束后降至室温,观察到水倒吸入集气瓶大于1/5.根据资料信息,小明知道镁条可以与空气中的氮气、二氧化碳发生反应,进而影响反应结果.镁条与氮气反应可以生成氮化镁(Mg3N2)和碳,请写出相应的化学方程式 .
探究结论:几种物质中,红磷是最适用于测定空气中氧气含量.
探究问题:红磷、白磷、木炭、镁条几种物质,哪种更适用于测定空气中氧气含量?
查阅资料:
①红磷、白磷对比情况
| 红磷 | 白磷 | |
| 状态 | 暗红色固体 | 蜡状固体 有毒 |
| 燃烧温度 | 240°C | 40°C |
探究过程:如下图所示,按照实验装置进行实验,探究几种物质测定空气中O2含量的可行性.
(1)红磷、白磷探究实验
小明认为选用红磷进行实验,其原因是
| 实验步骤 | 实验现象 | 结论和化学方程式 |
如图所示,将足量红磷放到燃烧匙中,点燃红磷,进行实验 |
空气中氧气约占 化学方程式 |
(3)若将实验药品改为镁条,反应结束后降至室温,观察到水倒吸入集气瓶大于1/5.根据资料信息,小明知道镁条可以与空气中的氮气、二氧化碳发生反应,进而影响反应结果.镁条与氮气反应可以生成氮化镁(Mg3N2)和碳,请写出相应的化学方程式
探究结论:几种物质中,红磷是最适用于测定空气中氧气含量.
根据初中化学知识,探究空气中氧气含量实验。小明根据所学内容,红磷、白磷、木炭、镁条都可以和氧气发生反应,但是哪种物质更适用于测定空气中氧气含量,小明进行如下探究。
【探究问题】红磷、白磷、木炭、镁条几种物质,哪种更适用于测定空气中氧气含量?
【查阅资料】
红磷、白磷对比情况
镁条可以与空气中多种物质反应,如N2、CO2等
【探究过程】如下图所示,按照实验装置进行实验,探究几种物质测定空气中O2含量的可行性。
(1)红磷、白磷探究实验小明认为选用红磷进行实验,其原因是 。
(2)若将实验药品改为木炭,反应结束后降至室温,打开止水夹,水不倒吸入集气瓶的原因是 。
(3)若将实验药品改为镁条,反应结束后降至室温,观察到水倒吸入集气瓶大于1/5。根据资料信息,小明知道镁条可以与空气中的氮气、二氧化碳发生反应,进而影响反应结果。镁条与氮气反应可以生成氮化镁(Mg3N2)和碳,请写出相应的化学方程式 。
【探究结论】几种物质中,红磷是最适用于测定空气中氧气含量。
【探究问题】红磷、白磷、木炭、镁条几种物质,哪种更适用于测定空气中氧气含量?
【查阅资料】
红磷、白磷对比情况
| | 红磷 | 白磷 |
| 状态 | 暗红色固体 | 蜡状固体 有毒 |
| 燃烧温度 | 240°C | 40°C |
【探究过程】如下图所示,按照实验装置进行实验,探究几种物质测定空气中O2含量的可行性。
(1)红磷、白磷探究实验小明认为选用红磷进行实验,其原因是 。
| 实验步骤 | 实验现象 | 结论和化学方程式 |
如图所示,将足量红磷放到燃烧匙中,点燃红磷,进行实验 | | 空气中氧气约占 化学方程式 |
(2)若将实验药品改为木炭,反应结束后降至室温,打开止水夹,水不倒吸入集气瓶的原因是 。
(3)若将实验药品改为镁条,反应结束后降至室温,观察到水倒吸入集气瓶大于1/5。根据资料信息,小明知道镁条可以与空气中的氮气、二氧化碳发生反应,进而影响反应结果。镁条与氮气反应可以生成氮化镁(Mg3N2)和碳,请写出相应的化学方程式 。
【探究结论】几种物质中,红磷是最适用于测定空气中氧气含量。
根据初中化学知识,探究空气中氧气含量实验。小明根据所学内容,红磷、白磷、木炭、镁条都可以和氧气发生反应,但是哪种物质更适用于测定空气中氧气含量,小明进行如下探究。
【探究问题】红磷、白磷、木炭、镁条几种物质,哪种更适用于测定空气中氧气含量?
【查阅资料】
红磷、白磷对比情况
| | 红磷 | 白磷 |
| 状态 | 暗红色固体 | 蜡状固体 有毒 |
| 燃烧温度 | 240°C | 40°C |
【探究过程】如下图所示,按照实验装置进行实验,探究几种物质测定空气中O2含量的可行性。
(1)红磷、白磷探究实验小明认为选用红磷进行实验,其原因是 。
| 实验步骤 | 实验现象 | 结论和化学方程式 |
如图所示,将足量红磷放到燃烧匙中,点燃红磷,进行实验 | | 空气中氧气约占 化学方程式 |
(2)若将实验药品改为木炭,反应结束后降至室温,打开止水夹,水不倒吸入集气瓶的原因是 。
(3)若将实验药品改为镁条,反应结束后降至室温,观察到水倒吸入集气瓶大于1/5。根据资料信息,小明知道镁条可以与空气中的氮气、二氧化碳发生反应,进而影响反应结果。镁条与氮气反应可以生成氮化镁(Mg3N2)和碳,请写出相应的化学方程式 。
【探究结论】几种物质中,红磷是最适用于测定空气中氧气含量。
根据初中化学知识,探究空气中氧气含量实验.小明根据所学内容,红磷、白磷、木炭、镁条都可以和氧气发生反应,但是哪种物质更适用于测定空气中氧气含量,小明进行如下探究.
探究问题:红磷、白磷、木炭、镁条几种物质,哪种更适用于测定空气中氧气含量?
查阅资料:
①红磷、白磷对比情况
| 红磷 | 白磷 | |
| 状态 | 暗红色固体 | 蜡状固体 有毒 |
| 燃烧温度 | 240°C | 40°C |
探究过程:如下图所示,按照实验装置进行实验,探究几种物质测定空气中O2含量的可行性.
(1)红磷、白磷探究实验
小明认为选用红磷进行实验,其原因是______.
| 实验步骤 | 实验现象 | 结论和化学方程式 |
如图所示,将足量红磷放到燃烧匙中,点燃红磷,进行实验 | ______ | 空气中氧气约占______ 化学方程式______ |
(3)若将实验药品改为镁条,反应结束后降至室温,观察到水倒吸入集气瓶大于1/5.根据资料信息,小明知道镁条可以与空气中的氮气、二氧化碳发生反应,进而影响反应结果.镁条与氮气反应可以生成氮化镁(Mg3N2)和碳,请写出相应的化学方程式______.
探究结论:几种物质中,红磷是最适用于测定空气中氧气含量.