题目内容
200克水溶解一定质量的氯化镁配制成溶液.取此溶液一半,加入一定质量20%的氢氧化钠溶液恰好完全反应,生成5.8克沉淀.
(1)求配制成氯化镁溶液的总质量.
(2)求反应后生成的溶液中溶质的质量分数.
(1)求配制成氯化镁溶液的总质量.
(2)求反应后生成的溶液中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:根据沉淀氢氧化镁的质量可以计算氯化镁的质量和生成的氯化钠的质量,进一步可以计算配制成氯化镁溶液的总质量和反应后生成的溶液中溶质的质量分数.
解答:解:(1)设参加反应的氯化镁的质量为x,氢氧化钠的质量为y,同时生成氯化钠的质量为z,
MgCl2+2NaOH=Mg(OH)2↓+2NaCl
95 80 58 117
x y 5.8g z
=
=
=
,
x=9.5g,y=8g,z=11.7g,
配制成的MgCl2溶液总质量为:(100g+9.5g)×2=219g,
答:配制成的MgCl2溶液总质量为219g.
(2)参加反应的氢氧化钠溶液质量为:8g÷20%=40g,
反应后生成的溶液中溶质的质量分数为:
×100%=8.1%,
答:反应后生成的溶液中溶质的质量分数为8.1%.
MgCl2+2NaOH=Mg(OH)2↓+2NaCl
95 80 58 117
x y 5.8g z
| 95 |
| x |
| 80 |
| y |
| 58 |
| 5.8g |
| 117 |
| z |
x=9.5g,y=8g,z=11.7g,
配制成的MgCl2溶液总质量为:(100g+9.5g)×2=219g,
答:配制成的MgCl2溶液总质量为219g.
(2)参加反应的氢氧化钠溶液质量为:8g÷20%=40g,
反应后生成的溶液中溶质的质量分数为:
| 11.7g |
| 109.5g+40g-5.8g |
答:反应后生成的溶液中溶质的质量分数为8.1%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
如图描述的过程中,属于化学变化的是( )
A、 干冰人工降雨 |
B、 研磨氧化铁样品 |
C、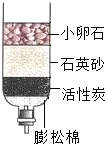 简易净水器净化水 |
D、 碎鸡蛋壳中加入食醋 |