题目内容
【题目】向amolFe2O3中滴加稀硫酸,随着硫酸的加入,有关量的变化见图,分析错误的是( )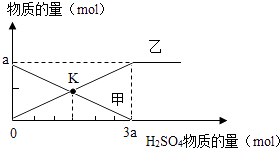
A.曲线甲表示氧化铁的物质的量
B.曲线乙表示生成水的物质的量
C.K点时溶液中铁元素的物质的量是amol
D.K点时硫酸铁和剩余氧化铁物质的量相等
【答案】B
【解析】解:向氧化铁中加入稀硫酸,发生反应:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,
A、向氧化铁中加入稀硫酸,发生反应:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O.氧化铁质量不断减少,反应完毕,氧化铁质量为0,曲线甲表示氧化铁的物质的量,故正确;
B、向amolFe2O3中滴加稀硫酸,随着硫酸的加入,水的物质的量不断增加,不会出现平线,故错误;
C、由Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
1 3
0.5mol 1.5mol
由图象可知:amolFe2O3中铁元素的物质的量是2amol,K点时氧化铁被消耗0.5amol,溶液中铁元素的物质的量是amol,故正确;
D、K点时氧化铁被消耗0.5mol,溶液中铁元素的物质的量是amol,剩余氧化铁物质的量为0.5amol×2=amol,点时硫酸铁和剩余氧化铁物质的量相等,故正确.
答案:B

【题目】根据如表回答问题.
温度(℃) | 20 | 40 | 50 | 60 | 80 | |
溶解度(g/100g水) | NaCl | 36.0 | 36.6 | 37.0 | 37.3 | 38.4 |
NH4Cl | 37.2 | 45.8 | 50.4 | 55.2 | 65.6 | |
KNO3 | 31.6 | 63.9 | 85.5 | 110 | 169 | |
(1)20℃时,溶解度最大的物质是
(2)50℃时,100g水中最多溶解NaClg
(3)量筒的局部示意见图,量取水时应沿视线(选填“a”或“b”)进行读数,视线(选填“a”或“b”)对应的读数较大.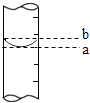
(4)A是80℃含有120g水的KNO3溶液,经过如下操作,得到102gKNO3固体.
Ⅰ.A溶液为(选填“饱和”或“不饱和”)溶液
Ⅱ.对以上过程的分析,正确的是(选填编号)
a.A到B的过程中,溶质质量没有改变
b.B中溶质与溶剂的质量比为169:100
c.开始析出KNO3固体的温度在60℃至80℃之间
d.A溶液的质量等于222g.
【题目】关于①、②两组对比实验的说法正确的是( )
①对比硫在空气和氧气中燃烧的剧烈程度 | ②探究二氧化碳能否与氢氧化钠反应 |
|
|
A.两个实验方案设计均合理
B.实验①中可观察到硫在空气中燃烧发出明亮的蓝紫色火焰
C.实验②中右瓶变瘪的程度更大
D.实验②反应后向右瓶中加入足量稀盐酸,可观察到冒气泡