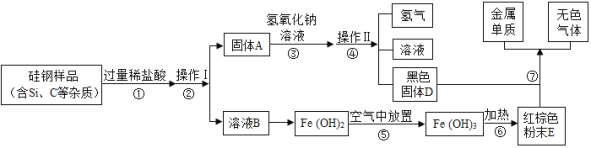
题目内容
【题目】某化学兴趣小组用一瓶含有少量氯化钠的硫酸钠固体样品,进行如图所示的实验。
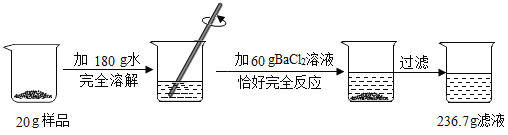
请根据以上信息计算(结果保留到小数点后一位):
(1)反应生成沉淀的质量为__________________________g。
(2)样品中硫酸钠的质量____________________。
(3)滤液中氯化钠的质量分数____________________。
【答案】23.3 14.2g 7.4%
【解析】
(1)由质量守恒定律,反应生成沉淀的质量为20g+180g+60g-236.7g=23.3g。
(2)设参加反应的硫酸钠的质量为x,生成氯化钠的质量为y
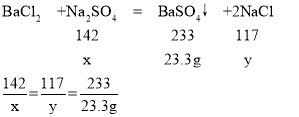
x=14.2g,y=11.7g
(3)滤液中氯化钠的质量分数为![]() ×100%≈7.4%。
×100%≈7.4%。
答:(1)反应生成沉淀的质量为23.3g;
(2)样品中硫酸钠的质量为14.2g;
(3)滤液中氯化钠的质量分数为7.4%。

练习册系列答案
相关题目