题目内容
【题目】取一定量的氯化钠与氢氧化钠的混合物,加一定量的水配制成100g溶液,然后向其中滴加氯化镁溶液,直至恰好完全反应,共消耗氯化镁溶液85.8g。过滤,得到180g质量分数为10%的氯化钠溶液。请计算:
(1) 生成沉淀的质量
(2) 原混合物中氢氧化钠的质量分数。(计算结果精确到0.1%)
【答案】(1)5.8g
(2)55.9%
【解析】
(1)沉淀的质量为反应前溶液的质量减去反应后溶液的质量,即沉淀的质量为混合物的水溶液质量与消耗的氯化镁的质量和减去最后得到的氯化钠溶液的质量:100g+85.8g-180g=5.8g。则生成沉淀的质量是5.8g。
(2)设原混合物中氢氧化钠的质量为x,生成氯化钠的质量为y
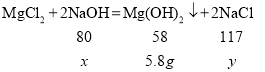
![]()
x=8g;y=11.7g
则原混合物中氯化钠的质量为:180×10%-11.7g=6.3g
故原混合物中氢氧化钠的质量分数为:![]()

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案【题目】某校兴趣小组的同学为了测定某石灰石中碳酸钙的质量分数,他们取该石灰石样品10g加入烧杯中,再把80g稀盐酸分四次加入,实验过程所得数据如下表(已知石灰石样品中含有的杂质既不溶于水,也不与稀盐酸反应):
实验次数 | 第 1 次 | 第 2 次 | 第 3 次 | 第 4 次 |
加入稀盐酸的质量/g | 20 | 20 | 20 | 20 |
剩余固体的质量/g | 6 | m | 1.2 | 1.2 |
分析表中数据,完成下列问题:
(1)表中m的数值为___;
(2)计算稀盐酸的溶质质量分数____。
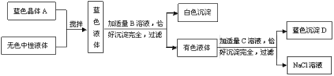
【题目】已知某种干电池的内部黑色糊状填充物含炭黑、二氧化锰、氯化铵和氯化锌。下列是回收利用干电池得到二氧化锰和氯化铵固体的流程:
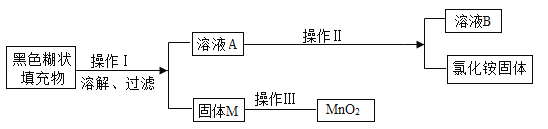
有关数据见表:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 | |
(1)操作I中用到的玻璃仪器有_____、玻璃棒和漏斗;
(2)固体M的成分为_____,操作Ⅲ的简便方法为_____。
(3)操作Ⅱ的过程包括、冷却结晶、过滤、洗涤、干燥。溶液B的溶质为_____;洗涤时最好选用下列物质中的_____作为洗涤液。
A 冰水 B 氯化铵饱和溶液 C 氯化锌饱和溶液 D 氯化钠饱和溶液
(4)施肥时不能将熟石灰与氯化铵混合施用的原因是_____(用化学方程式回答)。