题目内容
【题目】某矿泉水标签上印有主要矿物质成分如 Ca:20,K:39,Mg:3,Zn:0.06,F:0.02等,这里的Ca、K、Mg、Zn、F是指
A、单质 B、元素 C、金属离子 D、分子
【答案】B
【解析】
试题分析:在日常生活常接触到物品上的氟”、“钙”等指的均是元素。故选B。

 阅读快车系列答案
阅读快车系列答案【题目】某实验小组利用废硫酸液制备K2SO4并研究CaSO42H2O加热分解的产物.
(一)K2SO4的制备
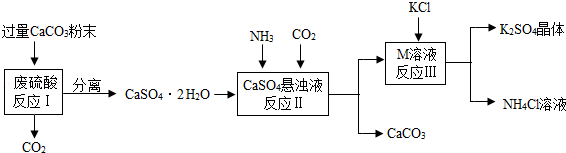
(1)将CaCO3研成粉末的目的是 .
(2)上述流程中可循环使用的物质有CO2和 (填写化学式).
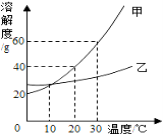
(3)反应Ⅲ中相关物质的溶解度如下表.你认为反应Ⅲ在常温下能实现的原因是 .
物质 | KCl | K2SO4 | NH4Cl | M |
溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
(4)不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的目的是 ;为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入 (选填序号,下同),振荡、静置,再向上层清液中滴加 ,观察现象即可判断.
a.AgNO3溶液
b.过量的BaCl2溶液
c.过量的Ba(NO3)2溶液
(二)研究CaSO42H2O加热分解的产物.
(5)分离所得的CaSO42H2O含有CaCO3,可用盐酸除去,该的化学反应方程式 .
(6)为了测定CaSO42H2O和CaCO3的质量比x:y,实验小组利用如图所示的装置(夹持仪器省略)进行实验.
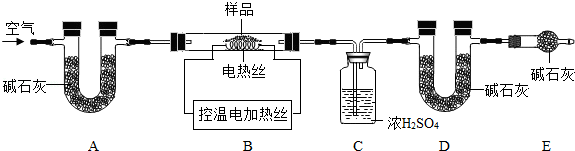
①实验前首先要 ,再装入样品.装置A的作用是 .
②已知CaSO42H2O在160℃生成CaSO4,1350℃时CaSO4开始分解;CaCO3在900℃时分解完全.现控制B装置温度900℃进行实验并采集了如下数据:
a.反应前玻璃管与样品的质量m1g
b.反应后玻璃管中固体的质量为m2g
c.装置C实验后增重m3g
d.装置D实验后增重m4g
某同学选用b、d或c、d数据组合求出x:y的值,若无装置E,则实验测定结果将 (填“偏大”、“偏小”或“无影响”).你认为还可选用上述的 (选填序号)两个数据组合也可求出x:y的值.
(7)CaSO42H2O受热会逐步失去结晶水.取纯净CaSO42H2O固体3.44g,放在(5)的实验装置B中进行加热,测定固体质量随温度的变化情况如图所示.①G点固体的化学式是 .
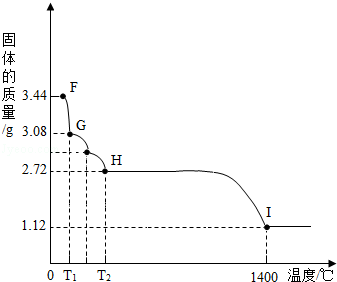
②将T2~1400℃温度段加热固体所产生的气体通入酸性KMnO4溶液中,溶液褪色,则H~I段发生反应的化学方程式为 .
【题目】小明家有包开启了的小苏打,久置在灶台上方,可能因受热而变质。小明为此开展了探究,请分析其过程完成填空。
【查阅资料】
① 2NaHCO3![]() Na2CO3 + CO2 ↑ + H2O
Na2CO3 + CO2 ↑ + H2O
② NaHCO3 + NaOH = Na2CO3 + H2O
③ 2NaHCO3 + Ca(OH)2 = CaCO3 ↓ + Na2CO3 + 2H2O
④ Ca(HCO3)2 + Na2CO3 = CaCO3 ↓ + 2 NaHCO3
⑤ Na2CO3受热不分解,NaHCO3、Ca(HCO3)2都能溶与水。
【假设猜想】
假设一:小苏打没有变质,化学成分为NaHCO3;
假设二:小苏打完全变质,化学成分为 ;
假设三:小苏打部分变质,化学成分为 。
【实验方案】
可选药品:①Ca(OH)2溶液 ②CaCl2溶液 ③NaOH溶液 ④稀盐酸
实验操作 | 实验现象 | 实验结论 |
操作一:取小苏打样品少量溶于足 量水后,加入过量的 (填药品编 号,下同),观察,如有沉淀,则继续进行下一步操作。 操作二:待操作一中反应充分后过 滤,并在滤液中加入过量的 ,观察。 | 操作一中无沉淀出现 | 假设一成立 |
假设二成立 | ||
假设三成立 |
【问题讨论】
有同学认为,取一定量样品直接加热,再将产生的气体通入澄清石灰水,根据实验现象,对上述三种假设的每一种是否成立都能进行判断。请评价这种方案是否合理 (填“是”或“否”),理由是 。