题目内容
【题目】某溶液可能含有盐酸、硫酸、硝酸钠、氯化铜中的一种或几种,为了探究其组成,向一定量的该溶液中逐滴加入氢氧化钡溶液,生成沉淀的质量与所加氢氧化钡溶液的质量之间的关系如图所示,据图分析解答问题:
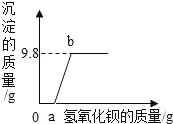
(1)0﹣a段没有沉淀产生,说明该溶液中一定没有的物质是_____;
(2)a﹣b段生成的沉淀一定含有_____;
(3)则原溶液中一定含有_____;’
(4)到达b点时所消耗的氢氧化钡溶液中溶质的质量_____17.1g(选填大于、等于或小于)
【答案】H2SO4 Cu(OH)2 HCl、CuCl2 大于
【解析】
由图象可知一开始加入氢氧化钡,没有沉淀,反应一段时间后又产生了沉淀,说明肯定有一种物质能与氢氧化钡产生沉淀,一开始不产生沉淀是因为其中含有酸,酸能把产生的沉淀溶解,所以加入的氢氧化钡先与酸反应,把酸反应完了再与另一种物质反应生成沉淀,酸不能是稀硫酸,硫酸与氢氧化钡反应生成硫酸钡沉淀,不溶于酸,所以图象中的沉淀应该从原点开始,所以只能是盐酸,所以与氢氧化钡产生沉淀只能是氯化铜溶液了,所以该混合物组成一定含有盐酸和氯化铜溶液,可能含有硝酸钠。
由分析可知:(1)溶液中一定不含有硫酸,化学式为:H2SO4;
(2)a﹣b段生成的沉淀一定含有氢氧化铜,化学式为:Cu(OH)2;
(3)原溶液中一定含有盐酸和氯化铜,化学式为:HCl、CuCl2;
(4)到达b点时,生成沉淀是9.8g,故生成9.8g氢氧化铜需要的氢氧化钡的质量为:

开始盐酸还要消耗氢氧化钡,故消耗氢氧化钡的质量大于17.1g。

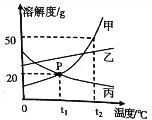
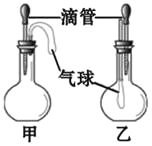
【题目】如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响)。则滴管和烧瓶中所用试剂可能是( )
甲 | 乙 | |
A. | 稀硫酸和铜片 | 水和硝酸铵固体 |
B. | 水和氢氧化钠固体 | AgNO3溶液和稀盐酸 |
C. | 双氧水和MnO2 | NaOH溶液和CO2 |
D. | Na2CO3溶液和稀硫酸 | 水和浓硫酸 |
A. AB. BC. CD. D
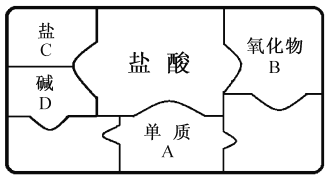
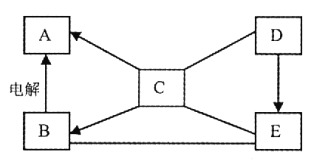
【题目】废铁屑的主要成分是铁,同时还有少量铁锈,动物饲料硫酸亚铁的生产工艺之一如下图所示
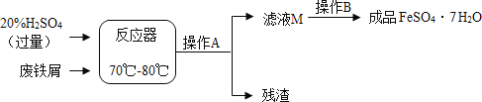
(1)写出在反应器中发生的化学反应方程式
①Fe2(SO4)3+Fe==3FeSO4;②_____;③_____
(2)滤液M中肯定含有的溶质的化学式是_____(填化学式)
(3)在实验室中完成操作A的玻璃仪器有玻璃棒、烧杯和_____
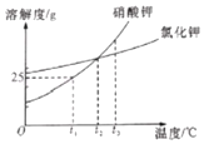
(4)滤液M经过操作B可得硫酸亚铁晶体(FeSO4·7H2O)
温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 | |||
溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 | |||
析出晶体 | FeSO47H2O | FeSO44H2O | FeSO4H2O | ||||||||||
根据上表,从滤液M得到硫酸亚铁晶体(FeSO4·7H2O)的最佳方案为:将M加热至_____℃,浓缩接近饱和后_____,再经过_____操作得到硫酸亚铁晶体
(5)将无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有氧化铁和两种硫的氧化物,试写出该反应的化学方程式_____