题目内容
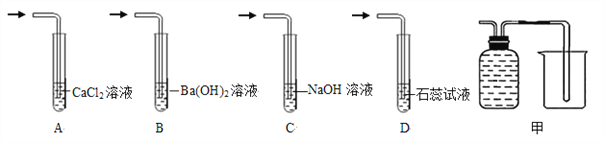
【题目】为了研究质量守恒定律,某兴趣小组设计了如图“白磷燃烧前后质量测定”的实验,请分析有关问题.

(1)装置:锥形瓶的底部铺有一层细沙,其作用是________.
(2)白磷燃烧:白磷燃烧过程中看到的现象是________.
(3)燃烧后称量:发现托盘天平指针偏向右边,造成这种现象的原因可能是________(只写一条).
(4)反思:白磷燃烧________(填“遵守”或“不遵守”)质量守恒定律,理由是________.
【答案】防止锥形瓶底部局部受热破裂产生白色的烟,气球胀大,后又缩小装置漏气遵守化学反应前后原子种类、数目和质量都不变
【解析】
(1)锥形瓶的底部铺有一层细沙,其作用是防止锥形瓶受热不均而炸裂;
(2)白磷燃烧过程中看到的现象是:产生白烟,气体遇热膨胀,气球胀大,后又缩小;
(4)发现托盘天平指针偏向右边,造成的原因可能是装置漏气,一部分五氧化二磷扩散到锥形瓶外或锥形瓶未冷却,气球仍在膨胀等;
(5)化学变化都遵循质量守恒定律,白磷燃烧属于化学变化遵守质量守恒定律,理由是参加反应的各物质的质量总和与生成的各物质的质量总和相等。

 名校课堂系列答案
名校课堂系列答案【题目】某校化学兴趣小组同学探究发现:铜绿[Cu2(OH)2CO3]受热分解后,除生成CO2和水蒸气外,试管中还有一些黑色粉末状固体.请回答下列问题:
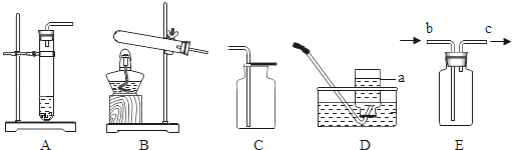
(1)写出标号a的仪器名称________
(2)实验室分解铜绿选用的发生装置为________ (填序号).初中实验室制取CO2________ 也可用E(长进短出),试分析其原因:________ .
(3)若向澄清的石灰水中通入少量CO2, 可观察到的现象:澄清石灰水变浑浊.用化学方程式表达:________ .
(4)充分反应后,兴趣小组对试管中的黑色粉末状状固体进一步探究
a.[提出问题]黑色固体是什么?
b.[猜想与假设]黑色固体可能是:Ⅰ.氧化铜Ⅱ.炭粉Ⅲ.________ .
c.[查阅资料]炭粉和氧化铜均为黑色固体.炭粉不与稀酸反应,也不溶于稀酸.而氧化铜可与稀酸反应而溶解.
d.[设计实验方案]向试管中的黑色固体滴加足量的试剂为________ (填序号)
(A.H2SO4 B.NaOH C.NaCl D.H2O),完成下列实验报告:
实验现象 | 实验结论 |
黑色固体全部溶解,溶液呈蓝色 | 猜想Ⅰ正确 |
________ | 猜想Ⅱ正确 |
________ | 猜想Ⅲ正确 |
如果猜想Ⅰ正确,猜想Ⅰ所发生反应的化学方程式为: ________ .
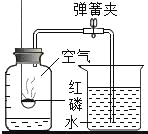
【题目】如图![]() 是“空气中氧气体积分数测定”实验的改进装置.主要操作是:在实际容积为
是“空气中氧气体积分数测定”实验的改进装置.主要操作是:在实际容积为![]() 的集气瓶里,先装进
的集气瓶里,先装进![]() 的水,再按图
的水,再按图![]() 连好仪器,按下热的玻璃棒,白磷立即被点燃.(白磷
连好仪器,按下热的玻璃棒,白磷立即被点燃.(白磷![]() 即燃烧,燃烧产物与红磷相同)
即燃烧,燃烧产物与红磷相同)
![]() 白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是________;若实验成功,最终集气瓶中水的体积约为________
白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是________;若实验成功,最终集气瓶中水的体积约为________![]() .
.
![]() 该实验可推论出氮气的性质为________.
该实验可推论出氮气的性质为________.
![]() 若将白磷换成炭粉,该实验能否获得成功?为什么?________.
若将白磷换成炭粉,该实验能否获得成功?为什么?________.
![]() 集气瓶里预先装进的
集气瓶里预先装进的![]() 水,在实验过程中起到哪些作用?(填写序号)
水,在实验过程中起到哪些作用?(填写序号)
![]() .加快集气瓶内气体冷却
.加快集气瓶内气体冷却![]() .液封导气管末端以防气体逸出
.液封导气管末端以防气体逸出![]() .吸收五氧化二磷
.吸收五氧化二磷
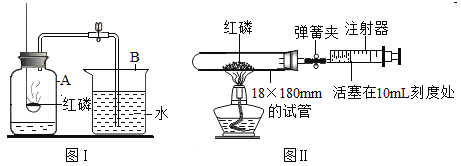
![]() 图
图![]() 是另一实验小组对测定空气中氧气含量实验的两套装置图,请结合图示回答有关问题.(已知铜和氧气在加热的条件下反应生成氧化铜固体)
是另一实验小组对测定空气中氧气含量实验的两套装置图,请结合图示回答有关问题.(已知铜和氧气在加热的条件下反应生成氧化铜固体)
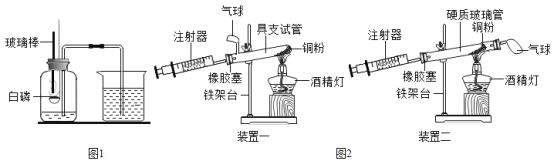
①根据下表提供的实验数据,完成如表
硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
|
|
| __________ |
②装置一和装置二中气球的位置不同,________(填“装置一”或“装置二”)更合理,理由是________.
③若实验测得的结果偏小(氧气的体积分数小于![]() ),可能的原因有哪些?________(列举两条).
),可能的原因有哪些?________(列举两条).