��Ŀ����
��1����֪ͭ����������FeCl3��Һ��Ӧ����Ӧ�Ļ�ѧ����ʽ�ֱ�Ϊ����Cu+2FeCl3=2FeCl2+CuCl2 ��Fe+2FeCl3=3FeCl2
����һ��ͭ�����Ļ�Ϸ�ĩ���뵽ʢ��һ����FeCl3��Һ���ձ��У���ַ�Ӧ���ձ���������������ʣ�࣬��ô�ձ��ڵĹ�����һ������ ���ձ��ڵ���Һ��һ�����е������� ��
��2����������ƽ�������ϸ���һֻ���������ձ�������ֻ�ձ���ֱ����50g������������Ϊ14.6%��ϡ���ᣮ����ƽ����ƽ����������ձ���Ͷ��һ������̼���ƹ��壬ǡ����ȫ��Ӧ���������ձ���Ͷ��6.4g����þ����Ʒ����Ʒ�����ʲ���þԪ�������ʲ���ϡ���ᷴӦ������ַ�Ӧ����ƽ�ٴ�ƽ�⣬��ý���þ��Ʒ��þ��������������Ϊ ��
���𰸡���������1�������ڽ������˳���У�λ����ǰ�Ľ����ܽ�λ�����Ľ�����������Һ���û������Լ�ͭ����������FeCl3��Һ��Ӧ�������������Һ�ijɷ֣�
��2�����ݻ�ѧ����ʽ�����֪��Ͷ��һ��������̼���ƹ��������ǡ����ȫ��Ӧ������6.2g����Ͷ��һ��������þ������ǡ����ȫ��Ӧ������2.2g ��������ƽ����Ҫʹ��������4g���������ձ����ܷ�Ӧ����������ȫ��Ӧ���������������ʲ����ٷ�����Ӧ����������������ӵ��������ɴ˿ɼ��������þ��Ʒ��þ������������
����⣺��1�������⣬��һ��ͭ�����Ļ�Ϸ�ĩ���뵽ʢ��FeCl3��Һ���ձ��У��ܷ����ķ�Ӧ�Т�Cu+2FeCl3=2FeCl2+CuCl2����Fe+2FeCl3=3FeCl2����Fe+CuCl2�TFeCl2+Cu��ͭ�����������Ȼ�����Ӧ�����Ȼ���������������Һ��һ�������Ȼ���������ַ�Ӧ�������������壬���ݷ�Ӧ�ķ���ʽ��֪һ������ͭ��������������ȷ�����ʿ��ܺ���������ͭ���ڣ�
��2����̼���������ᷴӦ�Ļ�ѧ����ʽ���ɵ�֪��
Na2CO3+2HCl�T2NaCl+H2O+CO2��
106 73 44
10.6g 50g×14.6%=7.3g 4.4g
����Ͷ��̼���Ƶ�����ʵ������=10.6g-4.4g=6.2g
���ݽ���þ�����ᷴӦ�Ļ�ѧ����ʽ���ɵ�֪��
2HCl+Mg�TMgCl2+H2��
73 24 2
7.3g 2.4g 0.2g
����Ͷ�����þ������ʵ������=2.4-0.2=2.2g
���ǡ����ȫ��Ӧ����ƽ�����������������������������6.2g-2.2g=4g�����ԣ�Ҫʹ��ƽ��Ȼ����ƽ�⣬��Ҫʹ��ƽ�Ҳ���������4g�������ձ��ڿ��Է�����Ӧ����������ȫ��Ӧ���������������ʲ��ٷ�����Ӧ����������������ӵ����������μӷ�Ӧ���������ԣ��ý���þ��Ʒ��þ��������������Ϊ��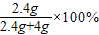 =37.5%��
=37.5%��
�ʴ�Ϊ����1��Cu��FeCl2����2��37.5%��
���������ڷ�Ӧ�ų����壬���ӹ�������������ձ�������������ʵ�����ӵ�������ʵ����������Ϊ�������������ų����������IJ
��2�����ݻ�ѧ����ʽ�����֪��Ͷ��һ��������̼���ƹ��������ǡ����ȫ��Ӧ������6.2g����Ͷ��һ��������þ������ǡ����ȫ��Ӧ������2.2g ��������ƽ����Ҫʹ��������4g���������ձ����ܷ�Ӧ����������ȫ��Ӧ���������������ʲ����ٷ�����Ӧ����������������ӵ��������ɴ˿ɼ��������þ��Ʒ��þ������������
����⣺��1�������⣬��һ��ͭ�����Ļ�Ϸ�ĩ���뵽ʢ��FeCl3��Һ���ձ��У��ܷ����ķ�Ӧ�Т�Cu+2FeCl3=2FeCl2+CuCl2����Fe+2FeCl3=3FeCl2����Fe+CuCl2�TFeCl2+Cu��ͭ�����������Ȼ�����Ӧ�����Ȼ���������������Һ��һ�������Ȼ���������ַ�Ӧ�������������壬���ݷ�Ӧ�ķ���ʽ��֪һ������ͭ��������������ȷ�����ʿ��ܺ���������ͭ���ڣ�
��2����̼���������ᷴӦ�Ļ�ѧ����ʽ���ɵ�֪��
Na2CO3+2HCl�T2NaCl+H2O+CO2��
106 73 44
10.6g 50g×14.6%=7.3g 4.4g
����Ͷ��̼���Ƶ�����ʵ������=10.6g-4.4g=6.2g
���ݽ���þ�����ᷴӦ�Ļ�ѧ����ʽ���ɵ�֪��
2HCl+Mg�TMgCl2+H2��
73 24 2
7.3g 2.4g 0.2g
����Ͷ�����þ������ʵ������=2.4-0.2=2.2g
���ǡ����ȫ��Ӧ����ƽ�����������������������������6.2g-2.2g=4g�����ԣ�Ҫʹ��ƽ��Ȼ����ƽ�⣬��Ҫʹ��ƽ�Ҳ���������4g�������ձ��ڿ��Է�����Ӧ����������ȫ��Ӧ���������������ʲ��ٷ�����Ӧ����������������ӵ����������μӷ�Ӧ���������ԣ��ý���þ��Ʒ��þ��������������Ϊ��
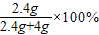 =37.5%��
=37.5%���ʴ�Ϊ����1��Cu��FeCl2����2��37.5%��
���������ڷ�Ӧ�ų����壬���ӹ�������������ձ�������������ʵ�����ӵ�������ʵ����������Ϊ�������������ų����������IJ

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ

 ���͡�
���͡� ���ֱ��ʾ���ֲ�ͬ��ԭ�ӣ����б�ʾ���������
���ֱ��ʾ���ֲ�ͬ��ԭ�ӣ����б�ʾ���������