题目内容
【题目】科学探究很奇妙!在一次实验中,小明不小心把硫酸铜溶液滴加到了盛有5%过氧化氢的溶液中,发现立即有大量气泡产生。硫酸铜溶液中有三种粒子(![]() 、
、![]() 、
、![]() ),小明想知道硫酸铜溶液中的哪种粒子能使双氧水分解的速率加快。请你和小明一起通过如图所示的三个实验完成这次探究活动,并回答有关问题。
),小明想知道硫酸铜溶液中的哪种粒子能使双氧水分解的速率加快。请你和小明一起通过如图所示的三个实验完成这次探究活动,并回答有关问题。
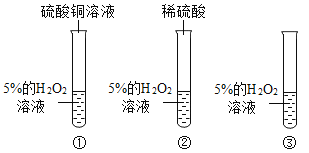
(1)你认为最不可能的是哪一种粒子?____;理由是_________。
(2)要证明另外两种粒子能否加快双氧水分解的速率,还需要进行实验②和③:在实验②中加入稀硫酸后,无明显变化,说明_______不起催化作用;在实验③中加入___________后,会观察到大量气泡,证明起催化作用的是_________。
(3)检验实验产生的气体的方法是_______________。
(4)小明如果要确定硫酸铜是催化剂,还需通过实验确认它在化学反应前后__________和 __________都不变。
【答案】![]() (或水分子) 5%过氧化氢的溶液中含有水分子
(或水分子) 5%过氧化氢的溶液中含有水分子 ![]() (或硫酸根离子) 硫酸铜溶液(或硝酸铜溶液或氯化铜溶液) 铜离子 把带火星的木条伸入试管,若木条复燃则是氧气 质量 化学性质
(或硫酸根离子) 硫酸铜溶液(或硝酸铜溶液或氯化铜溶液) 铜离子 把带火星的木条伸入试管,若木条复燃则是氧气 质量 化学性质
【解析】
(1)最不可能的是水分子;理由是:5%过氧化氢的溶液中含有大量水分子,但过氧化氢分子也没有加速分解;
(2)要证明另外两种粒子能否加快双氧水分解的速率,还需要进行实验②和③:硫酸中含有的微粒是氢离子和硫酸根离子,在实验②中加入稀硫酸后,无明显变化,说明硫酸根离子不起催化作用;在实验③中加入硫酸铜后,硫酸铜中含有硫酸根离子和铜离子,会观察到大量气泡,证明起催化作用的是:铜离子;
(3)过氧化氢分解产生水和氧气,氧气具有助燃性,检验氧气的方法是:把带火星的木条伸入试管,若木条复燃则是氧气;
(4)催化剂自身不参与反应,反应前后质量与化学性质不变;小明如果要确定硫酸铜是催化剂,还需通过实验确认它在化学反应前后化学性质和 质量都不变。

 习题精选系列答案
习题精选系列答案【题目】某白色固体可能由BaC12、NaOH、Na2CO3、Na2SO4中的一种或几种物质组成,某兴趣小组的同学为确定该白色固体的成分,进行了如下的实验探究,请你参与并回答相关问题。
I.初步探究:小金同学设计的实验过程及现象如下图所示。
(查阅资料)BaC12溶液显中性。

(初步结沦)(1)原白色固体中一定有的物质是_________,一定没有的物质是_________。
(2)M溶液中的溶质一定有__________,一定没有氯化钡。
(交流讨论)小英同学认为:无色溶液M变红色,说明溶液M中含有碱性物质,但不能由此推导出原固体物质中是否含有氢氧化钠。若要进一步确定,需对溶液M继续进行探究。为此同学们进行了如下的探究:
Ⅱ.继续探究:
(提出问题)无色溶液M中有氢氧化钠吗?
(猜想与假设)猜想一:有NaOH
猜想二:没有NaOH
(探究与结论)
实验步骤 | 实验现象 | 实验结论 |
A.取无色溶液M于试管中,加入过量的氯化钡溶液,振荡,静置 | _______________ | 证明溶液M中有碳酸钠并被除尽 |
B.取实验A所得上层清液于试管中,加入_______________。 | _____________ | 猜想一正确 |
在老师的指导下,同学们通过交流、讨论、实验,圆满地完成了这次探究活动。