题目内容
【题目】根据下图装置,回答下列有关问题:
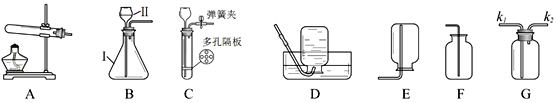
(1)写出仪器名称Ⅰ________________、Ⅱ________________。
(2)采用加热氯酸钾和二氧化锰的混合物制取氧气,可选用的发生装置是____________,
反应的化学方程式是___________________________________________, 选用D装置收集氧气时,下列实验操作中正确的是_______________(填序号)。
A. 将集气瓶注满水,用玻璃片盖住瓶口,倒立在盛水的水槽中
B. 等到气泡连续且均匀时,再将导管口移入集气瓶口
C. 收集满气体后,将集气瓶盖上玻璃片再移出水槽
D. 盖上毛玻璃片的集气瓶瓶口向下置于实验桌上
(3)可以用F收集二氧化碳的原因是________________________,检验二氧化碳气体是否收集满的方法是______________________________。
(4)若用G装置装满水收集氢气,氢气应从__________进。(选“k1”或“k2”)。
【答案】 锥形瓶 长颈漏斗 A 2KClO3![]() 2KCl+3O2↑ ABC 密度比空气大 将燃着的木条置于集气瓶口 k2
2KCl+3O2↑ ABC 密度比空气大 将燃着的木条置于集气瓶口 k2
【解析】(1)根据常见仪器的结构,可知仪器Ⅰ为锥形瓶、Ⅱ为长颈漏斗;
(2)装置A适用于加热氯酸钾和二氧化锰的混合物制取氧气,反应的化学方程式是2KClO3![]() 2KCl+3O2↑, 选用D装置排水法收集氧气时,首先将集气瓶注满水,用玻璃片盖住瓶口,倒立在盛水的水槽中,等到气泡连续且均匀时,再将导管口移入集气瓶口,待收集满气体后,将集气瓶盖上玻璃片再移出水槽,最后将盖上毛玻璃片的集气瓶瓶口向上置于实验桌上,故答案为ABC;
2KCl+3O2↑, 选用D装置排水法收集氧气时,首先将集气瓶注满水,用玻璃片盖住瓶口,倒立在盛水的水槽中,等到气泡连续且均匀时,再将导管口移入集气瓶口,待收集满气体后,将集气瓶盖上玻璃片再移出水槽,最后将盖上毛玻璃片的集气瓶瓶口向上置于实验桌上,故答案为ABC;
(3)CO2的密度比空气大,则可以用F收集二氧化碳,将燃着的木条置于集气瓶口,若木条熄灭,则说明二氧化碳气体收集满;
(4)若用G装置装满水收集氢气,氢气应从k2进,水从k1排出。

【题目】以下是空气污染指数与质量级别、质量状况的对应关系:
空气污染指数 | 0~50 | 51~100 | 101~200 | 201~300 | >300 |
空气质量状况 | 优 | 良 | 轻度污染 | 中度污染 | 重度污染 |
空气质量级别 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ |
根据“中国国家环境监测”数据,2015年10月12日,重庆空气污染指数为99,根据以上信息,判断重庆当天空气质量级别和空气质量状况分别是
A.Ⅰ级 优 B.Ⅱ级 良
C.Ⅲ级 轻度污染 D.Ⅴ级 重度污染