题目内容
【题目】为测定混有少量氯化钠的纯碱中碳酸钠的质量分数,做如下实验:准确称量样品12g,向其中加入68g稀盐酸,恰好完全反应,称量所得溶液质量为75.6g。请计算: (计算结果精确到小数点后一位)
(1)反应生成二氧化碳的质量___________。
(2)纯碱样品中碳酸钠的质量分数____________。
(3)所得溶液中溶质的质量____________。
【答案】4.4g 88.3% 13.1g
【解析】
(1)根据质量守恒定律,生成二氧化碳气体的质量为:![]()
(2)设反应的Na2CO4的质量为x。
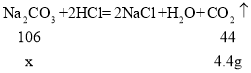
![]()
x=10.6g
纯碱样品中碳酸钠的质量分数= ![]()
答:纯碱样品中碳酸钠的质量分数为88.3%。
(3)解:设生成的NaCl质量为y
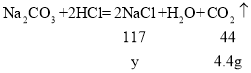
![]()
y=l1.7g
所得溶液中NaCI的质量为:![]()
答:所得溶液中NaCI的质量为13.1 g

练习册系列答案
 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目