��Ŀ����
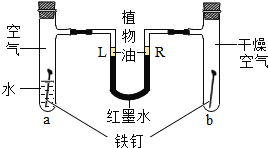
����Ŀ��Ϊ�ⶨ�����������ĺ�����С��ͬѧ����������·�����ѡ��ʵ���ݻ�Ϊ 40mL ���Թ�����Ӧ�������������İ������Թܣ�����Ƥ�������Թܣ�ͨ��������ʵ���ݻ�Ϊ 60mL �����Ժܺõ���Ͳע���������ͼ��ʵ��װ�á������ʵ���ܹ�����С���������������У��Ұ�����ռ�������Ƥ������������ڵ�������������Բ��ƣ���ش��������⣺

��1��ʵ��ǰ�����ɼУ���ע��������ǰ�ش� 20mL �̶ȴ�̯��15mL �̶ȴ���Ȼ���ɿ��֣����������ܷ���ֻ 20mL �̶ȴ�����˵����_____��
��2�����ȼн����ɼУ��þƾ��Ƽ��Ȱ��ף�ȼ�ս������ȵ��Թ���ȴ�����ɿ����ɼУ�д����ȼ�յĻ�ѧ����ʽ��_____���ɹ۲쵽�������У�_____��
��3������ʹ�õ��ɼУ��þƾ��Ƽ��Ȱ��ף���ַ�Ӧֱ��ȼ�ս��������Թ���ȴ��ɹ۲쵽ע�����Ļ���ͣ��_____�̶ȴ���
���𰸡�װ�õ������Ժ� 4P+5O2![]() 2P2O5 ���������˶���ֹͣ��12mL�Ŀ̶ȴ� Լ8mL
2P2O5 ���������˶���ֹͣ��12mL�Ŀ̶ȴ� Լ8mL
��������
��1�����ɼУ���ע��������ǰ�ش�20mL�̶ȴ�����15mL�̶ȴ���Ȼ���ɿ��֣����������ܷ�����20mL�̶ȴ���˵������װ�ö���©����װ�õ������Ժã�����װ�õ������Ժá�
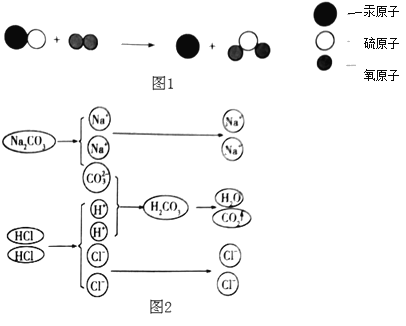
��2�����������ڵ�ȼ�������·�Ӧ�������������ף��ʷ�Ӧ�Ļ�ѧ����ʽдΪ��4P+5O 2 ![]() 2P2O5��
2P2O5��
���ȼн����ɼУ��þƾ��Ƽ��Ȱ��ף���ʱ����ȼ�����ĵ���ֻ���Թ��ڵ������������ΪΪ40mL��![]() ��8mL�����Ի��������˶�����ͣ��20mL��8mL��12mL�Ŀ̶ȴ���������������˶���ֹͣ��12mL�Ŀ̶ȴ���
��8mL�����Ի��������˶�����ͣ��20mL��8mL��12mL�Ŀ̶ȴ���������������˶���ֹͣ��12mL�Ŀ̶ȴ���
��3������ʹ�õ��ɼУ��þƾ��Ƽ��Ȱ��ף�����ʵ�����ĵ������Թ�40mL��ע������20mL�������������Ϊ��40mL+20mL����![]() ��12mL�����Ի���Ӧͣ��20mL��12mL��8mL�Ŀ̶ȴ�������Լ8mL��
��12mL�����Ի���Ӧͣ��20mL��12mL��8mL�Ŀ̶ȴ�������Լ8mL��

 ��У����ϵ�д�
��У����ϵ�д�