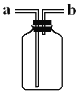
题目内容
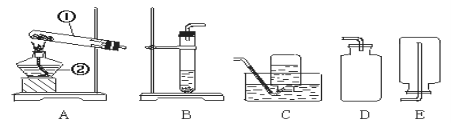
【题目】现提供如下装置,你会选择怎样的发生装置和收集装置来制取二氧化碳呢?
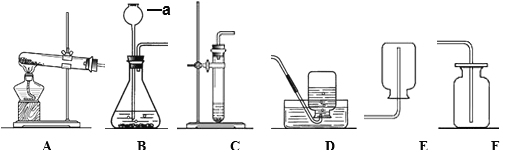
(1)仪器a的名称是______;实验时使用它的优点是________;实验室制取CO2时,应选择的发生装置是______(填字母,下同)和收集装置是 _____,实验室制取CO2的原理是用大理石或石灰石和稀盐酸反应,化学反应方程式为_________。
(2)实验室制取CO2时,不能用浓盐酸,原因是__________。
(3)CO2验满的方法是 _________ 。
(4)(常温下,硫化氢(H2S)是一种有臭鸡蛋气味的气体:验室可用硫化亚铁(FeS)固体和稀硫酸反应制得,该反应的方程式为FeS+H2SO4=H2S↑+FeSO4.实验室制取硫化氢气体应选用的发生装置是 ________(填字母),选择的依据是___________
(5)B装置除了能实验室制取CO2外,还能用来制取_________气体,制取该气体的化学反应方程式为 __________
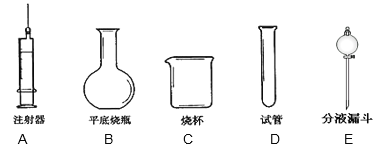
(6)制取CO2时还可选用下列装置中的__________仪器可取得更好的效果。
【答案】长颈漏斗 添加液体方便 B或C E CaCO3+2HCl= CaCl2+H2O+CO2↑ 有挥发性,使CO2不纯 燃着的木条放到集气瓶口,若熄灭,则满 B或C 固液常温制取气体 氧气(O2) 2H2O2![]() 2H2O+O2↑ A或E
2H2O+O2↑ A或E
【解析】
(1)仪器a是长颈漏斗,其作用是为了方便添加液体试剂;实验室制取CO2时,是利用大理石或石灰石与稀盐酸来反应,属于固液常温型,所以选择装置B来制取,二氧化碳的密度比空气大,能溶于水,所以只能用向上排空气法来收集;大理石或石灰石的主要成分是碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,化学反应方程式为:CaCO3+2HCl= CaCl2+H2O+CO2↑;
(2)浓盐酸具有挥发性,若使用浓盐酸制取二氧化碳则会造成挥发出HCl使二氧化碳不纯;
(3)根据二氧化碳验满的方法是:用燃着的木条放在瓶口,如果木条熄灭则说明瓶内已收集满二氧化碳;
(4)据题中提供的制取硫化氢的药品和反应条件,选择的发生装置属于固液常温型的B装置;
(5)装置B适用于固液常温下制取气体,如用过氧化氢在二氧化锰的催化作用下来制取氧气,同时生成水,化学反应方程式为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(6)注射器、分液漏斗代替长颈漏斗的优点是:可以控制液体药品流量,从而节约药品,控制反应速率等。

 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案【题目】某密闭容器中有X、氧气和二氧化碳三种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表。根据表中信息,判断下列说法正确的是( )
物质 | X | O2 | CO2 | H2O |
反应前质量/g | 23 | 70 | 1 | 0 |
反应后质量/g | 0 | 待测 | 45 | 27 |
A. 该反应为分解反应
B. 反应生成的CO2和H2O的质量比为45︰27
C. 表中“待测”值为5
D. X中含有氧元素