题目内容
【题目】比较是经常使用的一种学习方法。
(1)用下列字母序号填空:
A.镁粉 b.氮气 c. 石墨
①用作烟花, ②用作粮食保护气 ,③用于生产铅笔芯。
(2)请选用“>”或“<”或“=”填空。
① 空气中气体成分的体积分数:氮气稀有气体;
② 熔点:武德合金(铋、铅、锡、镉等金属合金)铅;
③ 2g硫粉在2g氧气中完全燃烧后生成二氧化硫的质量4g;
④ 相同的两段细铁丝在空气中生锈的速率:干燥的铁丝用食盐水浸过的铁丝;
⑤ 生铁中的含碳量钢中的含碳量;
⑥ 通常状况下的液体体积:100mL酒精与100mL水混合200mL。
【答案】
(1)a,b,c
(2)>,<,=,<,<,<
【解析】解:(1)镁燃烧发出耀眼的强光,常用作烟花;氮气化学性质稳定,用作粮食保护气,隔绝氧气防止食品因缓慢氧化而变质;石墨很软,且是黑色,在纸上划过会留下黑色痕迹,用于生产铅笔芯;(2)空气中各成分的含量按体积分数计算,氮气占78%,氧气占21%,稀有气体占0.94%;硫燃烧时,参加反应的硫和氧气的质量比为1:1,2g硫粉在2g氧气中完全燃烧后生成二氧化硫的质量等于4g;盐溶液会加速锈蚀,相同的两段细铁丝在空气中生锈的速率:干燥的铁丝小于用食盐水浸过的铁丝;生铁中的含碳量大于钢中的含碳量;酒精和水都是由分子构成的,分子间是有间隔的,100mL酒精与100mL水混合,所得液体体积小于200ml。
所以答案是:(1)a,b,c;(2)![]() ,
,![]() ,
,![]() ,
,![]() ,
,![]() ,
,![]() 。
。
【考点精析】根据题目的已知条件,利用空气的成分及各成分的体积分数和合金的定义与性能的相关知识可以得到问题的答案,需要掌握空气是混合物:O2约占1/5,可支持燃烧;N2约占4/5,不支持燃烧,也不能燃烧,难溶于水;合金:由一种金属跟其他一种或几种金属(或金属与非金属)一起熔合而成的具有金属特性的物质.一般说来,合金的熔点比各成分低,硬度比各成分大,抗腐蚀性能更好.

【题目】鸡蛋主要由蛋壳、蛋壳膜、蛋白、蛋黄等几个部分组成,其中蛋壳的主要成分是CaCO3 , 里面覆盖一层蛋壳膜。我校兴趣小组的同学为此开展了以下探究活动:
【提出问题1】
(1)鸡蛋白中含有的营养成分是。
(2)【查阅资料】
A.蛋壳是经过自然形成。科学手段检测蛋壳中含CaCO3约82%—85%,蛋白质15%—17%,并含多种微量元素;
b.蛋壳膜中蛋白质约占90%—93%。
【提出问题2】
蛋壳中的CaCO3含量是多少呢?小华拟将该蛋壳放在空气中充分灼烧完成测定;小明拟通过蛋壳与稀盐酸反应完成测定。请你参与他们的探究。
【设计方案】他们分别称取12.0 g蛋壳设计了以下不同的实验方案:
小华的方案:
称取12.0 g蛋壳研磨成粉末置于通风橱中,灼烧至质量不再减少,再称量剩余固体的质量为7.16g。则:产生的CO2质量g,蛋壳中的CaCO3的质量分数为%(结果保留到小数点后一位)。
(3)小明的方案:小明设计了如下图所示的实验装置。(已知其他成分均不与稀盐酸反应,装置内试剂均足量)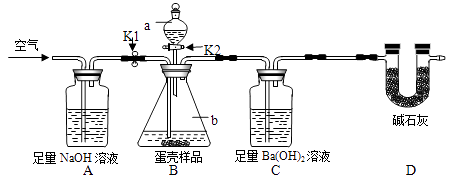
【实验步骤】
① 出编号仪器的名称:a , b;
② 按上图连接好装置后,并;
③ 向B装置中加入蛋壳样品后,先通入空气一会儿;
④ K1 , K2(填“打开”或“关闭”),向蛋壳样品中滴入10%的盐酸,直到B中为止(填实验现象);
⑤ 再通入一会儿空气,目的是;
⑥ 将装置C中的固液混合物过滤、洗涤、干燥后称量其质量;
⑦ 重复上述实验。
(4)【实验数据】重复实验,3次数据记录如下:
实验次数 | 实验1 | 实验2 | 实验3 |
装置C中沉淀质量(g) | 19.68 | 19.75 | 19.67 |
【实验分析及数据处理】
① 上述数据能否用托盘天平称量。(填“能”或“不能”)
② 若无A装置,直接通入空气,则测定结果将。(填“偏大”、“偏小”或“不变”)
③ 实验重复3次的目的是。
④ 请利用3次实验数据的平均值,计算该蛋壳中的CaCO3含量(已知:BaCO3相对分子量为197,结果保留到小数点后一位)。(请写出具体的计算过程,该空2分)
(5)【实验反思】
①下列各项措施中,能提高小明测定准确度的是(填字母序号)。
A.在装置A、B之间增加盛有浓硫酸的洗气瓶
B.缓缓滴加稀盐酸
C.在装置B、C之间增加盛有饱和NaHCO3的洗气瓶
②大家讨论后,一致认为小明的方案更合理,你认为小华方案存在较大误差的原因主要是。

