题目内容
氨气是一种无色有刺激性气味、极易溶于水、密度比空气小的气体.某学习小组在探究活动中要制取一定量的氨气,该小组查阅资料后,得知以下两种方法可以制取氨气:
第一种方法:氮气与氢气在高温、高压、催化剂的条件下生成氨气;
第二种方法:氯化铵固体和熟石灰粉末在加热条件下生成氨气.
(1)该小组同学没有选择第一种方法制取氨气的原因是
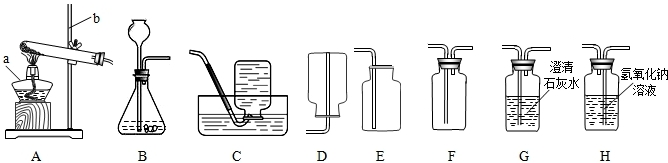
(2)在如图所示装置中,制取氨气的装置是
(3)实验室制取气体选择发生装置的依据是
出用该装置制取O2的后果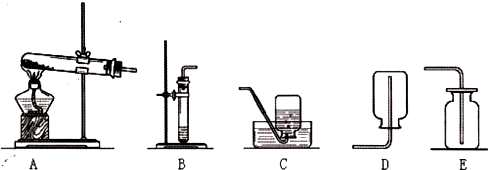
第一种方法:氮气与氢气在高温、高压、催化剂的条件下生成氨气;
第二种方法:氯化铵固体和熟石灰粉末在加热条件下生成氨气.
(1)该小组同学没有选择第一种方法制取氨气的原因是
反应条件难以实现
反应条件难以实现
.(2)在如图所示装置中,制取氨气的装置是
A
A
,理由是反应物是固体,且需要加热
反应物是固体,且需要加热
;收集氨气的装置是D
D
,理由是氨气极易溶于水、密度比空气小
氨气极易溶于水、密度比空气小
.(3)实验室制取气体选择发生装置的依据是
反应物的状态和反应条件
反应物的状态和反应条件
,用排空气法收集气体,导管应伸入集气瓶底部,否则会造成收集的气体不纯
会造成收集的气体不纯
; 小明同学建议用装置B做“H2O2分解制取O2”实验,遭到大多数同学的一致反对,请你说出用该装置制取O2的后果
反应速度太快,不宜收集
反应速度太快,不宜收集
,如果必须用该装置,需要对药品进行怎样的处理将二氧化锰放于试管,通过分液漏斗逐滴滴加过氧化氢溶液
将二氧化锰放于试管,通过分液漏斗逐滴滴加过氧化氢溶液
.
分析:(1)氮气与氢气在高温、高压、催化剂反应,该条件在实验室不易达到;
(2)根据氯化铵和熟石灰反应条件和反应物状态选择发生装置,并据氨气的密度和溶解性选择收集装置;
(3)根据反应物的状态和反应条件选择发生装置,用排空气法收集气体,导管应伸入集气瓶底部,是为了排尽集气瓶内的空气,防止收集的气体不纯;
实验室用H2O2溶液制取O2,反应速度太快,如果直接将二者混合,不宜收集;如果必须用该装置,将二氧化锰放于试管,可通过分液漏斗逐滴滴加过氧化氢溶液,可得到平稳的氧气流.
(2)根据氯化铵和熟石灰反应条件和反应物状态选择发生装置,并据氨气的密度和溶解性选择收集装置;
(3)根据反应物的状态和反应条件选择发生装置,用排空气法收集气体,导管应伸入集气瓶底部,是为了排尽集气瓶内的空气,防止收集的气体不纯;
实验室用H2O2溶液制取O2,反应速度太快,如果直接将二者混合,不宜收集;如果必须用该装置,将二氧化锰放于试管,可通过分液漏斗逐滴滴加过氧化氢溶液,可得到平稳的氧气流.
解答:解:(1)氮气与氢气在高温、高压、催化剂反应,该条件在实验室不易达到;
(2)氯化铵和熟石灰反应需要加热,属于固体加热型,故选择发生装置A,氨气极易溶于水、密度比空气小,所以只能用向下排空气法收集;
(3)选择发生装置通常依据反应物的状态和反应条件,用排空气法收集气体,导管应伸入集气瓶底部,是为了排尽集气瓶内的空气,防止收集的气体不纯;实验室用H2O2溶液制取O2,反应速度太快,如果直接将二者混合,不宜收集;如果必须用该装置,将二氧化锰放于试管,可通过分液漏斗逐滴滴加过氧化氢溶液,可得到平稳的氧气流;
故答案为:(1)反应条件难以实现;
(2)A;反应物是固体,且需要加热;D;氨气极易溶于水、密度比空气小;
(3)反应物的状态和反应条件;会造成收集的气体不纯;反应速度太快,不宜收集;将二氧化锰放于试管,通过分液漏斗逐滴滴加过氧化氢溶液.
(2)氯化铵和熟石灰反应需要加热,属于固体加热型,故选择发生装置A,氨气极易溶于水、密度比空气小,所以只能用向下排空气法收集;
(3)选择发生装置通常依据反应物的状态和反应条件,用排空气法收集气体,导管应伸入集气瓶底部,是为了排尽集气瓶内的空气,防止收集的气体不纯;实验室用H2O2溶液制取O2,反应速度太快,如果直接将二者混合,不宜收集;如果必须用该装置,将二氧化锰放于试管,可通过分液漏斗逐滴滴加过氧化氢溶液,可得到平稳的氧气流;
故答案为:(1)反应条件难以实现;
(2)A;反应物是固体,且需要加热;D;氨气极易溶于水、密度比空气小;
(3)反应物的状态和反应条件;会造成收集的气体不纯;反应速度太快,不宜收集;将二氧化锰放于试管,通过分液漏斗逐滴滴加过氧化氢溶液.
点评:本题考查了常见气体的制取并在学习的基础上进行拓展运用,能够考查学生的分析问题的能力.

练习册系列答案
相关题目