题目内容
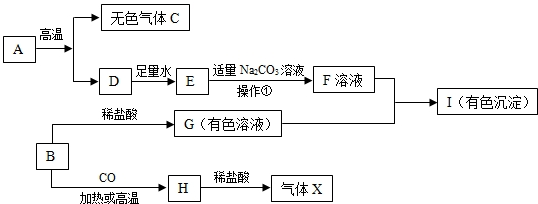
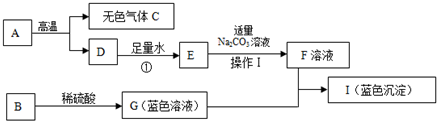
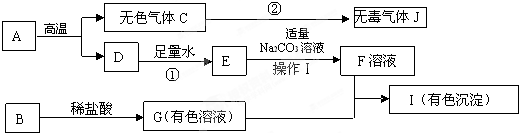
下列框图中的物质均为初中化学常见的物质,其中A是建筑材料的主要成分,B属于氧化物,下图是它们之间的相互转化关系.请回答:
(1)A物质中所含阳离子的符号为
(2)得到F溶液的操作Ⅰ的名称为:
(3)写出反应②中气体C转化为气体J的化学方程式:
(4)指出反应①的基本类型是

(1)A物质中所含阳离子的符号为
Ca2+
Ca2+
,物质E的俗名为熟石灰
熟石灰
;(2)得到F溶液的操作Ⅰ的名称为:
过滤
过滤
.(3)写出反应②中气体C转化为气体J的化学方程式:
6CO2+6H2O
C6H12O6+6O2
| ||
| 光 |
6CO2+6H2O
C6H12O6+6O2
若I是红褐色沉淀,请写出G+F→I的化学方程式:
| ||
| 光 |
FeCl3+3NaOH=Fe(OH)3↓+3NaCl
FeCl3+3NaOH=Fe(OH)3↓+3NaCl
(4)指出反应①的基本类型是
化合
化合
反应.分析:(1)根据A是建筑材料的主要成分,所以A就是碳酸钙,碳酸钙高温会生成二氧化碳和氧化钙,所以C是二氧化碳,D是氧化钙,氧化钙和水生成氢氧化钙,所以E是氢氧化钙,氢氧化钙和碳酸钠会生成碳酸钙沉淀和氢氧化钠,所以F就是氢氧化钠,将推出的物质验证即可;
(2)根据分离固体和液体的操作进行分析;
(3)根据(1)推出的反应物、生成物书写方程式;根据I是红褐色沉淀和放反应反应原理,可知I是氢氧化铁,G就是氯化铁,B就是氧化铁进行分析;
(4)依据该反应的特征分析解答即可;
(2)根据分离固体和液体的操作进行分析;
(3)根据(1)推出的反应物、生成物书写方程式;根据I是红褐色沉淀和放反应反应原理,可知I是氢氧化铁,G就是氯化铁,B就是氧化铁进行分析;
(4)依据该反应的特征分析解答即可;
解答:解:(1)A是建筑材料的主要成分,且高温时能分解生成无色气体C和D,根据常见物质的性质可知此物质为碳酸钙,含有的阳离子是Ca2+则C为二氧化碳,D为氧化钙,氧化钙与水反应会生成氢氧化钙,俗称熟石灰;
(2)氧化钙与水发生化合反应生成氢氧化钙,氢氧化钙与碳酸钠反应生成氢氧化钠和碳酸钙沉淀,要把碳酸钙沉淀分离出去得到F溶液,可以采用过滤的方法;
(3)由以上分析可知②是二氧化碳发生的光合作用过程,其方程式为:6CO2+6H2O
C6H12O6+6O2;反应I是红褐色沉淀说明I是氢氧化铁,则G中含有铁离子,而G是由氧化物与盐酸反应生成,说明G是氯化铁,所以G+F→I的反应为氯化铁与氢氧化钠的反应,方程式为:FeCl3+3NaOH=Fe(OH)3↓+3NaCl;
(4)①是氧化钙和水生成氢氧化钙的过程,该反应的反应物是两种生成物是一种,所以是化合反应;
故答案为:(1)Ca2+;熟石灰;(2)过滤;
(3)6CO2+6H2O
C6H12O6+6O2;FeCl3+3NaOH=Fe(OH)3↓+3NaCl;(4)化合;
(2)氧化钙与水发生化合反应生成氢氧化钙,氢氧化钙与碳酸钠反应生成氢氧化钠和碳酸钙沉淀,要把碳酸钙沉淀分离出去得到F溶液,可以采用过滤的方法;
(3)由以上分析可知②是二氧化碳发生的光合作用过程,其方程式为:6CO2+6H2O
| ||
| 光 |
(4)①是氧化钙和水生成氢氧化钙的过程,该反应的反应物是两种生成物是一种,所以是化合反应;
故答案为:(1)Ca2+;熟石灰;(2)过滤;
(3)6CO2+6H2O
| ||
| 光 |
点评:本题为框图式推断题,解题关键是找准解题的突破口,并从突破口出发,探求知识间的内在联系,应用多种思维方式,进行严密的分析和逻辑推理,推出符合题意的结果.

练习册系列答案
相关题目