题目内容
(2005?茂名)对于Mg2+和Mg两种粒子比较,下列说法不正确的是( )
分析:根据两种粒子的特点可以看出它们都是镁元素形成的不同微粒,则它们的质子数相同,但它们的电子数不同,据此分析解答.
解答:解:A、由于Mg2+是Mg原子失去2个电子形成的,故两种粒子的核外电子数不同;
B、元素的化学性质取决于微粒的最外层电子数,Mg2+和Mg两者最外层电子数不同,所以化学性质不同;
C、Mg2+和Mg两种粒子都是同种元素形成的微粒,故其质子数相同;
D、原子和离子都能够构成物质,故镁离子与镁原子都可构成物质.
故选:AB.
B、元素的化学性质取决于微粒的最外层电子数,Mg2+和Mg两者最外层电子数不同,所以化学性质不同;
C、Mg2+和Mg两种粒子都是同种元素形成的微粒,故其质子数相同;
D、原子和离子都能够构成物质,故镁离子与镁原子都可构成物质.
故选:AB.
点评:本题难度不大,掌握原子和离子的相互转化的实质并能灵活运用是正确解答本题的关键.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案
相关题目
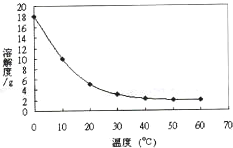
 (2005?茂名)如图为某物质的溶解度曲线图,对于该物质,下列说法不正确的是( )
(2005?茂名)如图为某物质的溶解度曲线图,对于该物质,下列说法不正确的是( )