题目内容
【题目】已知碳酸亚铁在隔绝空气的条件下,受热易分解生成氧化亚铁和二氧化碳;在空气中加热,则生成氧化铁和二氧化碳。某化学兴趣小组用下图所示的装置模拟炼铁过程,并测定某样品中碳酸亚铁的含量(该装置气密性良好,B中氢氧化钠溶液足量)。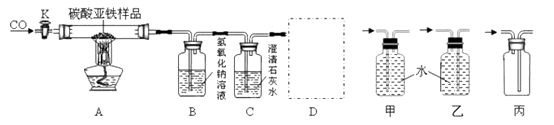 实验过程中,先打开K通入一氧化碳再加热;装置A中固体质量不再减少后,停止加热,待装置A冷却到室温后关闭K;实验测得装置A中固体质量减少了a g,装置B中液体质量增加了b g。请回答下列问题:
实验过程中,先打开K通入一氧化碳再加热;装置A中固体质量不再减少后,停止加热,待装置A冷却到室温后关闭K;实验测得装置A中固体质量减少了a g,装置B中液体质量增加了b g。请回答下列问题:
(1)写出装置A中发生反应的化学方程式、。
(2)能判断生成的二氧化碳全部被装置B吸收的依据是:装置B且装置C。
(3)若生成的二氧化碳全部被装置B吸收,不考虑水的蒸发且该样品中所含杂质不参加反应,则a b(填“>”、“=”或“<”)。
(4)D处为收集尾气的装置,应选择装置(填“甲”、“乙”或“丙”)。
【答案】
(1)FeCO3![]() FeO+CO2↑;FeO+CO
FeO+CO2↑;FeO+CO![]() Fe+CO2
Fe+CO2
(2)质量增加;澄清石灰水不变浑浊
(3)<
(4)乙
【解析】(1)装置A中发生的反应有:碳酸亚铁受热分解生成氧化亚铁和二氧化碳,一氧化碳和氧化亚铁在高温的条件下反应生成铁和二氧化碳,化学方程式为:FeCO3![]() FeO+CO2↑,FeO+CO
FeO+CO2↑,FeO+CO![]() Fe+CO2;
Fe+CO2;
(2)判断生成的二氧化碳全部被装置B吸收的依据是:装置B的质量增加并且C中澄清的石灰水不变浑浊;
(3)根据质量守恒定律,A中的质量减少是碳酸亚铁反应,最后变成铁,所以减少的质量是碳酸亚铁中的碳元素和氧元素的质量和,而装置B中增加的质量是二氧化碳的质量,二氧化碳中碳元素和氧元素,不但有碳酸亚铁中的,也有一氧化碳中的,所以装置B中增加的质量大于A中减少的质量;
(4)一氧化碳有毒,排放到空气中会污染大气,所以要进行尾气处理,能收集尾气的装置是乙.
故答案为:(1)FeCO3![]() FeO+CO2↑;FeO+CO
FeO+CO2↑;FeO+CO![]() Fe+CO2;(2)质量增加;澄清石灰水不变浑浊;(3)<;(4)乙.装置A中发生的反应有:碳酸亚铁受热分解生成氧化亚铁和二氧化碳,一氧化碳和氧化亚铁在高温的条件下反应生成铁和二氧化碳,根据化学反应方程式的书写步骤写出化学方程式即可;
Fe+CO2;(2)质量增加;澄清石灰水不变浑浊;(3)<;(4)乙.装置A中发生的反应有:碳酸亚铁受热分解生成氧化亚铁和二氧化碳,一氧化碳和氧化亚铁在高温的条件下反应生成铁和二氧化碳,根据化学反应方程式的书写步骤写出化学方程式即可;
(2)二氧化碳能和澄清石灰水反应生成碳酸钙的沉淀;
(3)根据质量守恒定律判断即可;
(4)一氧化碳有毒,不能直接排放在空气中.

