题目内容
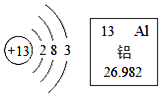
【题目】央视《每周质量报告》报道:一些不法企业用皮革废料熬制的工业明胶生产药用胶囊。在熬制明胶过程中添加重铬酸钾(K2Cr2O7),导致生产的药用胶囊重金属铬超标。根据化学式回答下列问题:
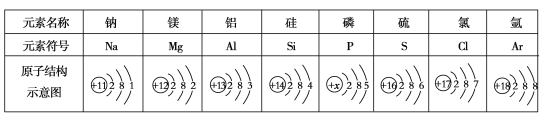
(1)请画出钾元素原子结构示意图_______。
(2)该物质由______种元素组成。
(3)钾、铬、氧三种元素的质量比为_______(要求填最简整数比)。
(4)铬元素的质量分数为________( 写出计算步骤, 结果保留到0.1%)。
【答案】![]() 三 39∶52∶56 35.4%(详见解析)
三 39∶52∶56 35.4%(详见解析)
【解析】
(1)在钾原子中,核内质子数为19,第一层上有2个电子,第二层上有8个电子,第三层上有8个电子,第四层上有1个电子,其原子结构示意图为![]() ;
;
(2)根据重铬酸钾(K2Cr2O7)的化学式可知,在重铬酸钾中,含有钾元素、铬元素、氧元素三种元素;
(3)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得重铬酸钾中钾、铬、氧元素的质量比=(39×2):(52×2):(16×7)=39:52:56;
(4)铬元素的质量分数=![]() 。
。

练习册系列答案
相关题目
【题目】张玲同学为测定汉白玉中碳酸钙的质量分数,称取5.55g研碎的汉白玉粉末进行四次高温加热、冷却、称量剩余固体的重复操作。记录数据如下:
操作次序 | 第一次 | 第二次 | 第三次 | 第四次 |
剩余固体质量(g) | 4.25 | 3.95 | 3.35 | 3.35 |
请计算:
(1)完全反应后产生的二氧化碳质量_____;
(2)汉白玉中碳酸钙的质量分数________。