题目内容
水是生命之源,人类的日常生活与工农业生产都离不开水.(1)在静置、过滤、吸附等方法中,能除去污水中臭味最有效的方法是
(2)硬水会给生活、生产带来许多麻烦.在日常生活中,可用
(3)
(4)经检验,水垢的主要成分是CaCO3和Mg(OH)2.某同学为测定水垢中CaCO3的质量分数,取200g水垢,并加入过量的稀盐酸完全反应后,测得生成CO2的质量为66g.请计算:CaCO3的相对分子质量为
分析:(1)静置是使水中悬浮固体沉降至水底部分的方法、过滤是把水中固体与水分离的方法,都不能除去污水中臭味,而吸附是除去水中异味、色素的常用方法;
(2)根据向硬水中加入肥皂水,泡沫较少,而把肥皂水加入纯水中泡沫丰富的不同现象,可使用肥皂水区分硬水与肥皂水;根据碳酸钙、金属铝与盐酸反应的规律,写出反应的化学方程式;
(3)根据水的化学式,由水中氢元素的质量分数及水的质量计算含一定量氢元素的水的质量;
(4)根据碳酸钙化学式计算碳酸的相对分子质量,根据碳酸钙与盐酸反应的化学方程式,由生成二氧化碳的质量计算水垢中碳酸钙的质量,利用碳酸钙质量与水垢质量比可计算该水垢中CaCO3的质量分数.
(2)根据向硬水中加入肥皂水,泡沫较少,而把肥皂水加入纯水中泡沫丰富的不同现象,可使用肥皂水区分硬水与肥皂水;根据碳酸钙、金属铝与盐酸反应的规律,写出反应的化学方程式;
(3)根据水的化学式,由水中氢元素的质量分数及水的质量计算含一定量氢元素的水的质量;
(4)根据碳酸钙化学式计算碳酸的相对分子质量,根据碳酸钙与盐酸反应的化学方程式,由生成二氧化碳的质量计算水垢中碳酸钙的质量,利用碳酸钙质量与水垢质量比可计算该水垢中CaCO3的质量分数.
解答:解:(1)吸附能除去水中异味及色素,能除去污水中臭味最有效的方法是吸附;
(2)硬水中钙、镁离子影响肥皂的起泡,可使用肥皂水区分纯水和硬水;碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O;铝也可以与盐酸反应,生成氯化铝和氢气,化学方程式为2Al+6HCl=2AlCl3+3H2↑;
(3)含有6g氢元素的水的质量=6g÷
×100%=54g
(4)CaCO3的相对分子质量=40+12+16×3=100
设水垢中碳酸钙的质量为x
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 44
x 66g
=
x=150g
该水垢中CaCO3的质量分数=
×100%=75%
故答案为:
(1)吸附;
(2)肥皂水;CaCO3+2HCl=CaCl2+CO2↑+H2O;2Al+6HCl=2AlCl3+3H2↑;
(3)54;
(4)100;75%.
(2)硬水中钙、镁离子影响肥皂的起泡,可使用肥皂水区分纯水和硬水;碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O;铝也可以与盐酸反应,生成氯化铝和氢气,化学方程式为2Al+6HCl=2AlCl3+3H2↑;
(3)含有6g氢元素的水的质量=6g÷
| 2 |
| 18 |
(4)CaCO3的相对分子质量=40+12+16×3=100
设水垢中碳酸钙的质量为x
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 44
x 66g
| 100 |
| x |
| 44 |
| 66g |
该水垢中CaCO3的质量分数=
| 150g |
| 200g |
故答案为:
(1)吸附;
(2)肥皂水;CaCO3+2HCl=CaCl2+CO2↑+H2O;2Al+6HCl=2AlCl3+3H2↑;
(3)54;
(4)100;75%.
点评:根据反应的化学方程式,可由反应放出气体的质量计算混合物中某组成物质的质量,进一步计算出混合物中该组成物质的质量分数.

练习册系列答案
相关题目

 水是生命之源,人类的日常生活和工农业生产都离不开水.右图甲是水电解实验的装置图,回答下列问题:
水是生命之源,人类的日常生活和工农业生产都离不开水.右图甲是水电解实验的装置图,回答下列问题: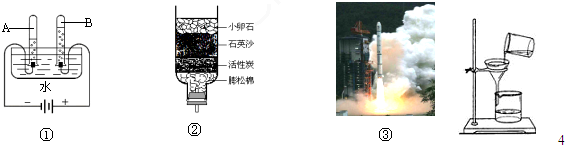
 水是生命之源,人类的日常生活离不开水.
水是生命之源,人类的日常生活离不开水.