题目内容
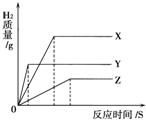
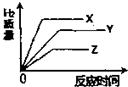
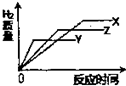
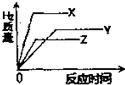
有等质量的X、Y、Z三种金属单质与足量的稀硫酸完全反应后,均生成+2价的化合物.它们的活泼性为:X>Z>Y,其相对原子质量大小为:Z>Y>X.下列各图中,能正确表示出反应时间与生成氢气质量大致关系的图为( )A.
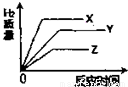
B.
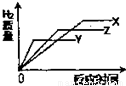
C.
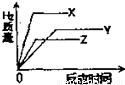
D.
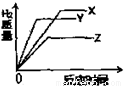
【答案】分析:根据金属与酸反应的关系分析.等质量的金属,活动性强的,与酸反应的速度就快,反应完用的时间就短,相同的时间内放出的氢气多.根据金属与酸反应产生氢气的质量公式:mH2= ×m金属,我们可以比较等质量的金属与酸反应生成氢气的多少小.
×m金属,我们可以比较等质量的金属与酸反应生成氢气的多少小.
解答:解:A、由于X、Y、Z三种金属活泼性为:X>Z>Y,与酸反应的速率是X>Z>Y,相同的时间内放出氢气的多少是:X>Z>Y.由图表A中可知,相同的时间内放出氢气的多少是:X>Y>Z.故A不正确;
B、由于X、Y、Z三种金属活泼性为:X>Z>Y,与酸反应的速率是X>Z>Y,由图表B中可知,与酸反应的速率是Y>Z>X.故B不正确;
C、由于X、Y、Z三种金属活泼性为:X>Z>Y,与酸反应的速率是X>Z>Y.由金属与酸反应产生氢气的质量公式:mH2= ×m金属及相对原子质量大小为:Z>Y>X可知,生成氢气的质量为:X>Y>Z,由图表B中可知,能正确表示出反应时间与生成氢气质量大致关系.故C正确;
×m金属及相对原子质量大小为:Z>Y>X可知,生成氢气的质量为:X>Y>Z,由图表B中可知,能正确表示出反应时间与生成氢气质量大致关系.故C正确;
D、由于X、Y、Z三种金属活泼性为:X>Z>Y,与酸反应的速率是X>Z>Y,由图表D中可知,与酸反应的速率是Y>Z>X.故D不正确.
故选C.
点评:该题考查了学生观察图表的能力,要求学生会根据图表判断金属的活动性,生成氢气质量的多少,反应速度的快慢,金属相对原子质量的大小.掌握住根据金属与酸反应产生氢气的质量公式.对以后的解题很有帮助.
 ×m金属,我们可以比较等质量的金属与酸反应生成氢气的多少小.
×m金属,我们可以比较等质量的金属与酸反应生成氢气的多少小.解答:解:A、由于X、Y、Z三种金属活泼性为:X>Z>Y,与酸反应的速率是X>Z>Y,相同的时间内放出氢气的多少是:X>Z>Y.由图表A中可知,相同的时间内放出氢气的多少是:X>Y>Z.故A不正确;
B、由于X、Y、Z三种金属活泼性为:X>Z>Y,与酸反应的速率是X>Z>Y,由图表B中可知,与酸反应的速率是Y>Z>X.故B不正确;
C、由于X、Y、Z三种金属活泼性为:X>Z>Y,与酸反应的速率是X>Z>Y.由金属与酸反应产生氢气的质量公式:mH2=
 ×m金属及相对原子质量大小为:Z>Y>X可知,生成氢气的质量为:X>Y>Z,由图表B中可知,能正确表示出反应时间与生成氢气质量大致关系.故C正确;
×m金属及相对原子质量大小为:Z>Y>X可知,生成氢气的质量为:X>Y>Z,由图表B中可知,能正确表示出反应时间与生成氢气质量大致关系.故C正确;D、由于X、Y、Z三种金属活泼性为:X>Z>Y,与酸反应的速率是X>Z>Y,由图表D中可知,与酸反应的速率是Y>Z>X.故D不正确.
故选C.
点评:该题考查了学生观察图表的能力,要求学生会根据图表判断金属的活动性,生成氢气质量的多少,反应速度的快慢,金属相对原子质量的大小.掌握住根据金属与酸反应产生氢气的质量公式.对以后的解题很有帮助.

练习册系列答案
相关题目
兴化地处里下河地区,河港纵横,水系发达.但河水中含有较多的碳酸氢钙[Ca(HCO3)2],水的硬度较大.(查阅资料:碳酸氢钙易溶于水.当溶有碳酸氢钙的水遇热时,溶解在水里的碳酸氢钙就会发生分解,生成碳酸钙沉积下来,这就形成了水垢Ca(HCO3)2△CaCO3↓+H2O+CO2↑).已知碳酸氢钠、碳酸氢钾、碳酸氢镁等物质均能在加热条件下发生类似的反应.而碳酸钠、碳酸钾则在通常情况下比较稳定,加热不分解.
请你根据上述信息完成下列各题:
(1)根据上述信息可知,水垢的主要成分是 .你能用什么方法来除去水垢?(用化学方程式表示) .
(2)若碳酸镁粉末中混有少量的碳酸氢镁,请写出除去杂质碳酸氢镁的方法(用化学方程式表示) .
(3)实验室有两包质量均为10.6g的固体,分别是碳酸钠和碳酸氢钠.现分别经如下处理:①充分加热 ②滴加足量的稀盐酸 ③将两步反应生成的气体全部收集后通入足量的澄清石灰水.则生成沉淀的质量 (填“相等”、“不相等”或“无法判断”).
(4)在加热条件下密闭容器内发生某一化学反应,现对反应体系内的X、Y、Z、Q四种物质进行测定,测得数据如下:
请回答下列问题:
①上表中的”待测数据”的数值是 .
②此密闭容器内反应类型属于 (填基本反应类型).
③若X是水,Q是能使澄清石灰水变浑浊的气体,且X、Y、Z、Q四种物质的化学计量数之比为1:1:2:1,则物质Y的相对分子质量为 .
(5)实验室制取二氧化碳时若不慎使用了浓盐酸,生成的气体中除混有水蒸气外还可能混有 气体,这是因为浓盐酸具有 性.
现要除去杂质气体,可采用如图所示的装置把不纯的气体进行洗气.
①不纯气体应从 (填“a”或“b”)端通入.
②若只需要把生成的气体干燥,可在瓶中盛放 .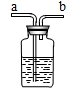
③可在瓶中盛放饱和的碳酸氢钠溶液除去另一种杂质气体.写出有关反应的化学方程式 .
请你根据上述信息完成下列各题:
(1)根据上述信息可知,水垢的主要成分是
(2)若碳酸镁粉末中混有少量的碳酸氢镁,请写出除去杂质碳酸氢镁的方法(用化学方程式表示)
(3)实验室有两包质量均为10.6g的固体,分别是碳酸钠和碳酸氢钠.现分别经如下处理:①充分加热 ②滴加足量的稀盐酸 ③将两步反应生成的气体全部收集后通入足量的澄清石灰水.则生成沉淀的质量
(4)在加热条件下密闭容器内发生某一化学反应,现对反应体系内的X、Y、Z、Q四种物质进行测定,测得数据如下:
| 物质 | X | Y | Z | Q |
| 反应前质量(g) | 40.0 | 4.6 | 37.8 | 0.0 |
| 反应后质量(g) | 43.6 | 待测数据 | 4.2 | 8.8 |
①上表中的”待测数据”的数值是
②此密闭容器内反应类型属于
③若X是水,Q是能使澄清石灰水变浑浊的气体,且X、Y、Z、Q四种物质的化学计量数之比为1:1:2:1,则物质Y的相对分子质量为
(5)实验室制取二氧化碳时若不慎使用了浓盐酸,生成的气体中除混有水蒸气外还可能混有
现要除去杂质气体,可采用如图所示的装置把不纯的气体进行洗气.
①不纯气体应从
②若只需要把生成的气体干燥,可在瓶中盛放

③可在瓶中盛放饱和的碳酸氢钠溶液除去另一种杂质气体.写出有关反应的化学方程式