题目内容
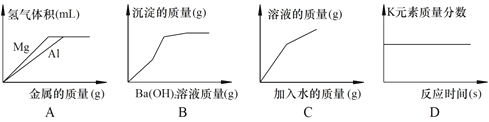
【题目】某同学做了三个实验,有关实验如图所示。
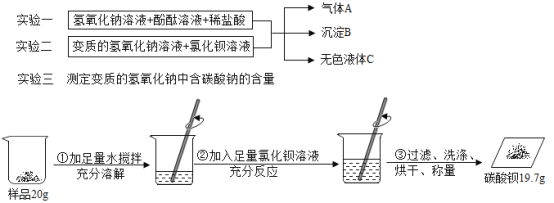
(1)实验一,向同一试管中依次加入三种溶液,观察到溶液的___________发生了改变;
(2)实验二,两种溶液混合发生反应,有关化学方程式为____________。
(3)实验一、实验二结束后将两反应容器内的物质混合在一起,产生气体A的化学反应可能是__________。(写出一个化学方程式即可)
(4)无色液体C,其溶质的组成情况有(除酚酞外)__________。
(5)根据实验三,计算该样品中含碳酸钠的质量分数为_________。
【答案】颜色 BaCl2+Na2CO3═BaCO3↓+2NaCl Na2CO3+2HCl=2NaCl+H2O+CO2↑(或BaCO3+2HCl=BaCl2+H2O+CO2↑) 氯化钠;氯化钠、氯化钡;氯化钠、碳酸钠 53%
【解析】
(1)实验一,向同一试管中依次加入三种溶液,观察到溶液的颜色发生了改变,即加入酚酞试液时溶液变红色,加入稀盐酸时,如果恰好完全反应或盐酸过量时溶液变成无色,稀盐酸不足时,溶液仍然是红色。
故填:颜色。
(2)实验二,两种溶液混合发生反应,氯化钡和碳酸钠(氢氧化钠变质会生成碳酸钠)反应生成碳酸钡沉淀和氯化钠,反应的化学方程式为:BaCl2+Na2CO3═BaCO3↓+2NaCl。
故填:BaCl2+Na2CO3═BaCO3↓+2NaCl。
(3)实验一、实验二结束后将两反应容器内的物质混合在一起,产生气体A的化学反应可能是:盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,和碳酸钡反应生成氯化钡、水和二氧化碳,盐酸和碳酸钠反应的化学方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑,盐酸和碳酸钡反应生成氯化钡、水和二氧化碳的化学方程式:BaCO3+2HCl=BaCl2+H2O+CO2↑。
故填:Na2CO3+2HCl=2NaCl+H2O+CO2↑(或BaCO3+2HCl=BaCl2+H2O+CO2↑)。
(4)无色液体C,其溶质的组成情况有(除酚酞外):氯化钠(盐酸和氢氧化钠、碳酸钠、碳酸钡恰好完全反应时);氯化钠、氯化钡(盐酸和碳酸钡部分反应时);氯化钠、碳酸钠(碳酸钠和盐酸部分反应时)。
故填:氯化钠;氯化钠、氯化钡;氯化钠、碳酸钠。
(5)设碳酸钠质量为x,

x=10.6g,
该样品中含碳酸钠的质量分数为:![]() ×100%=53%,
×100%=53%,
答:该样品中含碳酸钠的质量分数为53%。

【题目】碳酸氢铵是一种常用的化肥,小组同学对碳酸氢铵进行相关的探究:
[查阅资料](1)碳酸氢铵是一种白 色粒状晶体,有氨臭,易溶于水。
(2)氨气具有刺激性气味,极易溶于水。
[提出问题]碳酸氢铵有哪些化学性质?
[作出猜想]猜想一:碳酸氢铵能与酸反应;
猜想二:碳酸氢铵能与碱反应;
猜想三:碳酸氢铵易分解。
[设计与实验]
实验操作 | 实验现象 | 实验结论 | |
1 | _____ | 有气泡产生 | 猜想一正确 |
2 | 取少量碳酸氢铵样品与熟石灰混合研磨 | _____。 | 猜想二正确 |
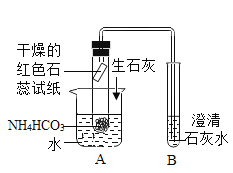
3 |
| 红色石蕊试纸变蓝,澄清石灰水变浑浊 | 猜想三正确, B中发生反应的化学方程式为_____。 |
[反思](1)实验3中向水中加入氧化钙的目的是_____。
(2)有同学对实验2的结论提出质疑:碳酸氢铵易分解产生有刺激性气味的气体,研磨会使温度升高,能加快碳酸氢铵分解,所以实验2的结论不严谨。
[补充探究]有同学为了进一步验证猜想二,进行如下实验:
实验操作 | 实验现象 |
①将碳酸氢铵溶液加入到氢氧化钙溶液中 | 有白 色沉淀生成,但没有气体逸出 |
②将碳酸氢铵溶液加入到氢氧化钠溶液中 | 有刺激性气味的气体生成 |
[分析]根据常见酸、碱、盐的溶解性分析,①实验中生成的白色沉淀是_____,实验中没有气体逸出可能的原因是_____。
[实验结论]三个猜想均正确。
[拓展应用]保存或使用碳酸氢铵时,需注意_____(写出一点)。