题目内容
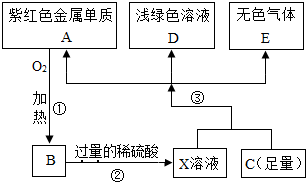 (2011?贺州)A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质.如图是它们之间的相互转化关系.请回答:
(2011?贺州)A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质.如图是它们之间的相互转化关系.请回答:(1)反应①产生的现象是
紫红色固体变为黑色
紫红色固体变为黑色
.(2)D中溶质的化学式是
FeSO4
FeSO4
.(3)物质C与X溶液中某种溶质反应有A 生成的化学方程式
Fe+CuSO4═Cu+FeSO4
Fe+CuSO4═Cu+FeSO4
.(4)若向X溶液中加入BaCl2溶液,则其中盐与盐之间发生反应的化学方程式为
BaCl2+CuSO4═BaSO4↓+CuCl2
BaCl2+CuSO4═BaSO4↓+CuCl2
.分析:金属单质C可以和X溶液反应生成浅绿色溶液D、紫红色金属A、无色气体E,所以可以判断D为硫酸亚铁溶液,E为氢气,而紫红色金属A为铜,所以X溶液为稀硫酸和硫酸铜铜盐溶液的混合溶液,可以据此结合题给的要求来完成解答即可.
解答:解:(1)金属单质C可以和X溶液反应生成浅绿色溶液D、紫红色金属A、无色气体E,所以可以判断D为硫酸亚铁溶液,E为氢气,而紫红色金属A为铜,所以X溶液为稀硫酸和硫酸铜铜盐溶液的混合溶液,所以反应①为铜和氧气的反应,该反应生成了氧化铜,氧化铜为黑色,所以可以观察到紫红色固体变为黑色;
(2)根据(1)中的解答可以知道溶液D为硫酸亚铁溶液,故其溶质为硫酸亚铁,其化学式为:FeSO4;
(3)根据(1)的解答可以知道物质C与X溶液中某种溶质反应有A生成,该反应为铁和硫酸铜溶液反应,其反应的化学方程式为:Fe+CuSO4═Cu+FeSO4;
(4)根据(1)的解答可以知道X中的盐为硫酸铜,所以加入氯化钡溶液后发生的反应为硫酸铜和氯化钡的反应,该反应的化学方程式为:BaCl2+CuSO4═BaSO4↓+CuCl2.
故答案为:(1)紫红色固体变为黑色;
(2)FeSO4;
(3)Fe+CuSO4═Cu+FeSO4;
(4)BaCl2+CuSO4═BaSO4↓+CuCl2.
(2)根据(1)中的解答可以知道溶液D为硫酸亚铁溶液,故其溶质为硫酸亚铁,其化学式为:FeSO4;
(3)根据(1)的解答可以知道物质C与X溶液中某种溶质反应有A生成,该反应为铁和硫酸铜溶液反应,其反应的化学方程式为:Fe+CuSO4═Cu+FeSO4;
(4)根据(1)的解答可以知道X中的盐为硫酸铜,所以加入氯化钡溶液后发生的反应为硫酸铜和氯化钡的反应,该反应的化学方程式为:BaCl2+CuSO4═BaSO4↓+CuCl2.
故答案为:(1)紫红色固体变为黑色;
(2)FeSO4;
(3)Fe+CuSO4═Cu+FeSO4;
(4)BaCl2+CuSO4═BaSO4↓+CuCl2.
点评:解答本题关键是要知道红色的金属单质是铜,知道浅绿色溶液是亚铁离子溶液,并要注意审题,在第②步骤中的过量稀硫酸也是解答本题的关键.

练习册系列答案
相关题目