题目内容
【题目】下图是某同学配制一定质量分数的氯化钠溶液的实验:
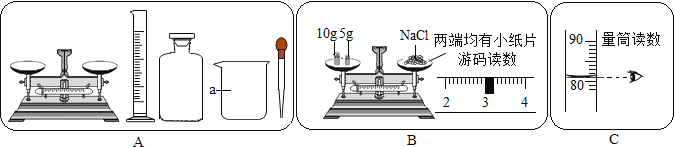
(1)图A中仪器a的名称___________;按实验要求,图A中还缺少的玻璃仪器是___________
(2)小红按图B所示的操作称取氯化钠,小明发现她的操作有错误你认为她的操作中的错误是_______________;她称取的氯化钠的实际质量是___________
(3)小红所取蒸馏水的体积如C图,小红原计划配制的氯化钠溶液的溶质质量分数为___________
【答案】烧杯 玻璃棒 砝码和物体放反了 12g 18%
【解析】
砝码和物体放反,药品实际质量=砝码质量游码质量。
(1)图1中仪器a的名称是烧杯。该图表示配制溶液全过程需用的所用仪器,称量氯化钠固体需要托盘天平、量取水的体积需要量筒,溶解时还会用到烧杯和玻璃棒。
(2)由图示可以看出托盘天平的使用错误,砝码和物体放反了,她称取的氯化钠的实验质量是![]() 。
。
(3)由图示中所示数据可得,每小格所表示的质量为1mL,水的体积为82mL,再由水的密度1g/mL,水的质量为![]() ,由托盘天平中砝码与游码的质量可知,该实验欲称药品质量为
,由托盘天平中砝码与游码的质量可知,该实验欲称药品质量为![]() ,溶液质量为
,溶液质量为![]() ,溶质质量分数为
,溶质质量分数为![]() 。
。

 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案【题目】兴趣小组的同学在社会实践基地发现一袋商标模糊的硝酸铵化肥。同学们要帮助基地的工作人员测定化肥中硝酸铵的含量,请你参与他们的探究活动。
(查阅资料)①铵态氮肥易溶于水。②铵态氮肥与碱反应产生氨气。③氨气易溶于水,溶液呈碱性。
(实验过程)小丽同学准确称取9.0 g硝酸铵化肥样品,与过量的氢氧化钙粉末混合,充分反应后,产生的氨气用足量的稀硫酸全部吸收,测得2分钟内稀硫酸溶液质量的变化,记录如下表所示(样品中的杂质不含氮元素,也不与氢氧化钙反应)。
时间/s | 0 | 20 | 40 | 60 | 80 | 100 | 120 |
溶液增加的质量/g | 0 | 0.7 | 1.2 | 1.5 | 1.6 | 1.7 | 1.7 |
(数据处理)
计算此化肥中硝酸铵的质量分数_____(写出计算过程)。
(反思交流)
化肥对粮食增产有着重要的作用,如何科学合理使用或贮存铵态氮肥,请你给工作人员提一条合理化建议_____。
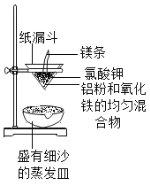
【题目】铝和氧化铁的反应:2A1+Fe2O3![]() Al2O3+2Fe,称为“铝热反应”(如图所示),引燃镁条,漏斗内的物质熔化,镁条燃尽,漏斗下端仍持续产生大量熔融物落入沙中,该熔融物可用于焊接铁轨。
Al2O3+2Fe,称为“铝热反应”(如图所示),引燃镁条,漏斗内的物质熔化,镁条燃尽,漏斗下端仍持续产生大量熔融物落入沙中,该熔融物可用于焊接铁轨。
(1)实验中镁条的作用是_____;氧化铁和铝粉都用粉末状的,原因是_____。
(2)某学习兴趣小组对所得熔融物的成分进行了探究。
(查阅资料)
①金属铝不但能和酸溶液(如稀盐酸)反应产生氢气,还能和强碱溶液(如氢氧化钠溶液)反应产生氢气。
②Al、A12O3、Fe、Fe2O3的熔点、沸点数据如下:
物质 | A1 | Al2O3 | Fe | Fe203 |
熔点/℃ | 660 | 2054 | 1535 | 1462 |
沸点/℃ | 2467 | 2980 | 2750 | - |
(实验猜想)
(3)某同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是:该反应放热能使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金。你认为他的解释是否合理?_____(填“合理”或“不合理”)。
(4)铝与稀盐酸反应的化学方程式为_____。
(5)请你根据已有知识找出一种验证产物中有Fe的最简单的方法:_____。
(实验验证)
(6)设计一个简单的实验方案,证明上述所得的熔融物中含有金属铝,请填写下列表格:
实验步骤 | 实验现象 | 实验结论 |
取少量冷却后的熔融物于试管中,加入_____ | _____ | 熔融物中含有铝 |


