题目内容
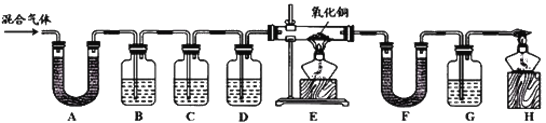
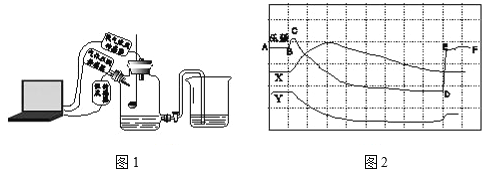
【题目】为了帮助同学们更好的理解空气中氧气含量测定的实验原理,老师利用传感器技术实时测定了实验装置(如图1)内的压强、温度和氧气浓度,三条曲线变化趋势如图2所示。
(1)红磷燃烧的化学反应方程式为________________________;
(2)X曲线表示的是____________(填“温度”或“氧气的浓度”);
(3)结合X、Y两条曲线,解释图2中BC段气压变化的原因是________________;
(4)实验中测得的数据如下:
测量 项目 | 实验前 | 实验后 | |
烧杯中水的体积 | 烧杯中剩余水的体积 | 瓶中剩余气体的体积 | |
体积/mL | 80.0 | 46.4 | 126.0 |
根据实验数据计算:测得的空气中氧气的体积分数为________(列出计算式即可)。
【答案】 4P+5O2![]() 2P2O5 温度 红磷燃烧放热温度升高,压强增大,同时消耗氧气,使气压减小。BC段燃烧放热造成的压强增大强于氧气减少造成的压强减小
2P2O5 温度 红磷燃烧放热温度升高,压强增大,同时消耗氧气,使气压减小。BC段燃烧放热造成的压强增大强于氧气减少造成的压强减小 ![]() ×100%
×100%
【解析】(1)红磷和氧气在点燃的条件下生成五氧化二磷;
(2)根据曲线变化分析;
(3)红磷燃烧放热,压强增大,消耗氧气,气压减小;
(4)根据金属解答。
解:(1)红磷和氧气在点燃的条件下生成五氧化二磷。化学方程式为:4P+5O2点燃2P2O5;
(2)刚开始反应时,红磷燃烧,温度升高,反应结束后,温度开始降低。故X曲线表示的是温度;
(3)结合X、Y两条曲线,解释图2中BC段气压变化的原因是:红磷燃烧放热温度升高,压强增大,同时消耗氧气,使气压减小。BC段燃烧放热造成的压强增大强于氧气减少造成的压强减小;
(4)空气中氧气的体积分数为: ![]() 。
。

【题目】为了测定液化气中丙烷(C3H8)在氧气不足时的燃烧产物,将一定量的丙烷和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
物质 | 丙烷 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 4.4 | 12.8 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
下列判断正确的是( )
A. X可能含有氢元素 B. X可能是该反应的催化剂
C. 表中a的值为5.6 D. X只含碳元素