题目内容
下列四个图象表示四种对应的操作过程,其中正确的是( )
A、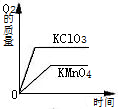 分别加热相同质量的KClO3和KMnO4 | B、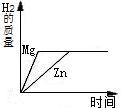 相同质量的镁、锌跟足量的稀硫酸制取氢气 | C、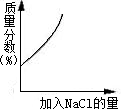 某温度下,在不饱和的食盐水中逐渐加入食盐晶体 | D、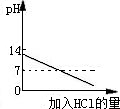 将盐酸滴入氢氧化钠溶液中,直至盐酸过量 |
分析:根据所学的制氧原理知识,加热相同质量的KClO3和KMnO4时KMnO4反应的速率快,故A错.根据方程式可以算出相同质量的镁、锌跟足量的稀硫酸制取氢气,镁最后产生的氢气多,故B错.根据某温度下,物质的溶液达到饱和状态后就不能继续溶解该物质,溶质的质量分数也就不会再改变,故C错.根据氢氧化钠溶液呈碱性,加盐酸,酸与碱会中和,PH逐渐下降,盐酸过量,PH小于7,故D对.从而可以正确作答.
解答:解:A、设 KClO3和KMnO4 的质量都为a,KClO3;生成氧气的质量为 x,KMnO4; 生成氧气的质量为y
2KClO3
2KCl+3O2 ↑ 2KMnO4
K2MnO4 +MnO2+O2 ↑
245 96 316 32
a x a y
═
═
x═
y═
∵
>
∴加热相同质量的KClO3和KMnO4时KClO3生成的氧气多,但是KMnO4较低温度下迅速放出氧气,而KClO3需较高温度且缓慢放出氧气.故A錯.
B、设镁和锌的质量都是 b,镁生成氢气的质量是m,锌生成氢气的质量是n
Mg+H2SO4═MgSO4+H2↑ Zn+H2SO4═ZnSO4+H2↑
24 2 65 2
b m b n
═
═
m═
n═
∵
>
∴相同质量的镁、锌跟足量的稀硫酸反,镁生成的氢气多.故B错
C、某温度下,在不饱和的食盐水中逐渐加入食盐晶体,食盐的质量分数逐渐增大,但是温度不变,当达到饱和时,食盐的质量分数就不会再改变,曲线不会一直呈上升趋势,故C错.
D、氢氧化钠溶液的PH大于7,将盐酸滴入氢氧化钠溶液中,酸性增大,PH减小,盐酸过量时,PH小于7,故D对.
故答案为D
2KClO3
| ||
| ||
245 96 316 32
a x a y
| 245 |
| 96 |
| a |
| x |
| 316 |
| 32 |
| a |
| y |
x═
| 96a |
| 245 |
| 32a |
| 316 |
∵
| 96a |
| 245 |
| 32a |
| 316 |
B、设镁和锌的质量都是 b,镁生成氢气的质量是m,锌生成氢气的质量是n
Mg+H2SO4═MgSO4+H2↑ Zn+H2SO4═ZnSO4+H2↑
24 2 65 2
b m b n
| 24 |
| 2 |
| b |
| m |
| 65 |
| 2 |
| b |
| n |
m═
| 2b |
| 24 |
| 2b |
| 65 |
∵
| 2b |
| 24 |
| 2b |
| 65 |
C、某温度下,在不饱和的食盐水中逐渐加入食盐晶体,食盐的质量分数逐渐增大,但是温度不变,当达到饱和时,食盐的质量分数就不会再改变,曲线不会一直呈上升趋势,故C错.
D、氢氧化钠溶液的PH大于7,将盐酸滴入氢氧化钠溶液中,酸性增大,PH减小,盐酸过量时,PH小于7,故D对.
故答案为D
点评:做这类图表题需认真阅读,筛选,提取图标中的有用信息,然后将所学知识与图表中的信息结合起来,即可进行计算或筛选.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
下列四个图象表示四种对应的操作过程,其中正确的是( )
A、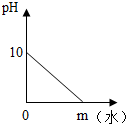 向pH=10的NaOH溶液中不断加水 | B、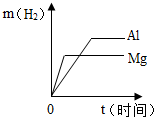 把相同质量的铝和镁放入足量的等质量等溶质质量分数的盐酸中 | C、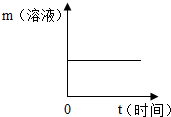 把铁棒放入硫酸铜溶液中 | D、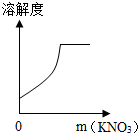 一定温度下,向10%的硝酸钾溶液中不断加入硝酸钾晶体 |

