题目内容
【题目】某化学小组利用CuSO4、FeSO4的混合溶液进行如下探究实验.
(1)写出铝与硫酸铜溶液反应的化学方程式 .
(2)向固体A中滴加稀盐酸,若有气泡产生,则A中一定含有的固体有哪些?若无气泡产生,则溶液B中一定含有的溶质有哪些?
(3)在实验时,某同学将铝片放入混合溶液中,发现有一种无色无味气体产生的“异常”现象.他猜想该气体可能为H2、CO2或SO2 . 请分别说明不可能是CO2和SO2的原因. 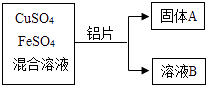
【答案】
(1)3CuSO4+2Al═3Cu+Al2(SO4)3
(2)答:铜和铁,硫酸亚铁和硫酸铝
(3)答:根据质量守恒定律,反应物中均不含碳元素,不可能生成CO2;SO2有刺激性气味,而该气体是无色无味的,故也不可能是SO2.
【解析】解:(1)铝和硫酸铜反应生成硫酸铝和铜,化学方程式为:3CuSO4+2Al═3Cu+Al2(SO4)3;(2)铝的金属活动性比铁、铜强,铝会先置换出溶液中的铜,然后再置换出铁,铁的活动性排在氢之前,铜不会与酸反应生成氢气,向固体A中滴加稀盐酸,有气泡产生,说明固体中一定含有铁、铜,可能含有铝;无气泡产生,说明固体中一定不含铁和铝,所以溶液中一定含有硫酸铝和硫酸亚铁;(3)由质量守恒定律可知,化学反应前后,元素种类不变,所以反应物中均不含碳元素,不可能生成CO2;SO2有刺激性气味,而该气体是无色无味的,故也不可能是SO2.
故答案为:(1)3CuSO4+2Al═3Cu+Al2(SO4)3;(2)铜和铁,硫酸亚铁和硫酸铝;(3)根据质量守恒定律,反应物中均不含碳元素,不可能生成CO2;SO2有刺激性气味,而该气体是无色无味的,故也不可能是SO2.
(1)根据铝和硫酸铜反应生成硫酸铝和铜进行分析;(2)根据铝的金属活动性比铁、铜强,铝会先置换出溶液中的铜,然后再置换出铁,铁的活动性排在氢之前,铜不会与酸反应生成氢气,向固体A中滴加稀盐酸,有气泡产生,说明固体中一定含有铁、铜,可能含有铝;无气泡产生,说明固体中一定不含铁和铝,所以溶液中一定含有硫酸铝和硫酸亚铁进行分析;(3)根据质量守恒定律可知,化学反应前后,元素种类不变进行分析.
