题目内容
 “嫦娥一号”的成功发射,使全国人民欢欣鼓舞.请同学们阅读下列航天技术中的化学短文并回答有关问题.
“嫦娥一号”的成功发射,使全国人民欢欣鼓舞.请同学们阅读下列航天技术中的化学短文并回答有关问题.材料一:2007年10月24日19时10分,“嫦娥一号”卫星发射成功.下图是中国月球探测工程标志图案.它以中国书法,抽象地勾勒出一轮圆月,一双脚印踏在其上,象征着月球探测的终极梦想.整体图形由一弧两点巧妙形成古文“月”字,同时代表“绕”、“落”、“回”三步走战略,此作品中国的意味十足,简洁而明朗,体现了传统和现代的完美结合.
材料二:人类要在月球活居住,首先离不开淡水和氧气,而月球上既没有水又没有空气.科学家发现月球的沙土中含有丰富的含氧钛铁矿,成分为TiO2、Fe2O3的混合物,将这些矿石利用CO来还原提炼单质钛和铁,若用氢气还原,可以得到淡水.将这些矿石通电,还可以从中分离出氧气.
请你从化学视角来见证这一伟大时刻:
(1)据了解,发射前8h开始加注火箭第三级使用的燃料液氢和液氧.其中液氧的主要作用是
(2)从铁生锈条件来分析,月球上铁制品
(3)现利用CO来还原TiO2、Fe2O3的混合物提炼单质钛和铁,装置如图所示,试回答:
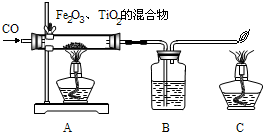
①写出A中CO还原TiO2的化学方程式
②就实验操作顺序的问题两位同学出现了分歧.
小月认为先通一段时间CO排空,然后再点燃C和A中的酒精灯.小亮认为这样做不好,他的理由是
小亮认为先点燃C和A中的酒精灯,然后再通CO,小月又提出反对,她的理由是
老师认为他们的反对意见都有一定道理.请你帮助这两位同学解决他们的困难,你的办法是
(4)小勇同学进一步探究钛铁矿中Fe2O3的质量分数,取10g钛铁矿样品进行实验,待完全反应后,用磁铁吸引铁粉,并称得铁粉的质量为5.6g,试求算钛铁矿中Fe2O3的质量分数为多少?
分析:(1)物质的性质决定用途,氧气不能燃烧,但能支持燃烧,氢气可燃,可作为燃料,密度小;
(2)从铁生锈需要的条件考虑,铁生锈需要氧气、水的参与,据此可判断月球上铁制品是否生锈;
(3)一氧化碳还原TiO2的化学方程式可参照一氧化碳还原氧化铁的方程式书写;在实验操作步骤上,一氧化碳应该是“早出晚归”,酒精灯应该“迟到早退”,一氧化碳有毒,在通一氧化碳之前应该先做好尾气处理.
(4)根据生成铁粉的质量,利用化学方程式即可求解.
(2)从铁生锈需要的条件考虑,铁生锈需要氧气、水的参与,据此可判断月球上铁制品是否生锈;
(3)一氧化碳还原TiO2的化学方程式可参照一氧化碳还原氧化铁的方程式书写;在实验操作步骤上,一氧化碳应该是“早出晚归”,酒精灯应该“迟到早退”,一氧化碳有毒,在通一氧化碳之前应该先做好尾气处理.
(4)根据生成铁粉的质量,利用化学方程式即可求解.
解答:解:(1)使用的燃料是液氢和液氧,其中液氧的主要作用是助燃,液氢是作燃料,由于氢气是最轻的气体,所以能大大减轻发射的质量,反应得化学方程式为2H2+O2
2H2O;
(2)铁生锈需要氧气、水的参与,而月球上既没有水又没有空气,所以月球上铁制品不易生锈;
(3)CO还原TiO2的化学方程式为:2CO+TiO2
Ti+2CO2,
小月认为先通一段时间CO排空,然后再点燃C和A中的酒精灯,没有考虑到一氧化碳有毒会污染空气;小亮认为先点燃C和A中的酒精灯,然后再通CO,没有考虑到一氧化碳可燃,与空气混合会发生爆炸;正确的操作顺序应该是:先通一段时间CO,同时点燃C处的酒精灯,排尽玻璃管内空气,然后再点燃A处的酒精灯(或先用气球收集尾气,然后再点燃酒精灯);
(4)设样品中Fe2O3的质量为x,则
3CO+Fe2O3
2Fe+3CO2
160 112
x 5.6g
=
x=8g
钛铁矿中Fe2O3的质量分数为:
×100%═80%
故答案为:(1)助燃、作燃料、密度小、2H2+O2
2H2O
(2)不易、月球上既没有水又没有空气
(3)①2CO+TiO2
Ti+2CO2、②CO有毒,对空气有污染;CO与容器内空气混合,点燃后可能会发生爆炸;先通一段时间CO,同时点燃C处的酒精灯,排尽玻璃管内空气,然后再点燃A处的酒精灯(或先用气球收集尾气,然后再点燃酒精灯)
(4)钛铁矿中Fe2O3的质量分数为80%.
| ||
(2)铁生锈需要氧气、水的参与,而月球上既没有水又没有空气,所以月球上铁制品不易生锈;
(3)CO还原TiO2的化学方程式为:2CO+TiO2
| ||
小月认为先通一段时间CO排空,然后再点燃C和A中的酒精灯,没有考虑到一氧化碳有毒会污染空气;小亮认为先点燃C和A中的酒精灯,然后再通CO,没有考虑到一氧化碳可燃,与空气混合会发生爆炸;正确的操作顺序应该是:先通一段时间CO,同时点燃C处的酒精灯,排尽玻璃管内空气,然后再点燃A处的酒精灯(或先用气球收集尾气,然后再点燃酒精灯);
(4)设样品中Fe2O3的质量为x,则
3CO+Fe2O3
| ||
160 112
x 5.6g
| 160 |
| 112 |
| x |
| 5.6g |
钛铁矿中Fe2O3的质量分数为:
| 8g |
| 10g |
故答案为:(1)助燃、作燃料、密度小、2H2+O2
| ||
(2)不易、月球上既没有水又没有空气
(3)①2CO+TiO2
| ||
(4)钛铁矿中Fe2O3的质量分数为80%.
点评:本题考查燃料的燃烧和一氧化碳还原矿石实验,在设计实验顺序上要注意坚持操作安全、环保的原则,先通一段时间一氧化碳是为了操作安全,先进性尾气处理是为了环保.(4)小题求质量分数时可以根据化学方程式求解,也可根据质量守恒定律,利用化学式求解,生成的铁完全来自氧化铁,氧化铁中铁元素的质量分数为:
×100%=70%,则
=8g,即氧化铁的质量为8g,再根据混合物总质量10g即可求出氧化铁的质量分数.
| 112 |
| 160 |
| 5.6g |
| 70% |

练习册系列答案
相关题目