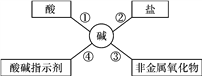
��Ŀ����
����Ŀ��(1)ijѧϰС��Ϊ�ⶨM���᳧�ŷŵķ�ˮ�е����Ậ����������ʵ�飺ȡ50 g��ˮ���ձ��У�������������Ϊ10%������������Һ(�ٶ���ˮ�������ɷֲ����������Ʒ�Ӧ)������ˮpH________(������7������7��������7��)ʱ��Ӧǡ����ȫ��������ĸ�����������Һ8 g���ݴ˼���÷�ˮ���������������Ϊ__________��
(2)M���᳧������ʯ�ҶԷ�ˮ���д�������������ƣ���֪M��ÿ�������ַ���������ˮ50�֣�����M��ÿ���������ܲ������ٶ�����ƣ�
���𰸡� ��7 1.96% (1)���ˮ�������������������Ϊx��
H2SO4��2NaOH===Na2SO4��2H2O
98 ��������80
50 g��x����8 g��10%
![]() ��
��![]() ������x��
������x��
(2)��ÿ������������CaSO4������Ϊy��
H2SO4��Ca(OH)2===CaSO4��2H2O
98��������������������136
50 t��1.96%������������y
![]() ��
��![]() ������y��1.36 t
������y��1.36 t
��(1)�÷�ˮ�������������������Ϊ1.96%��(2)ÿ���������ܲ���1.36������ơ�
��������(1)�������ƺ�ϡ���ᷢ���кͷ�Ӧʱ������ˮpH��7ʱ��Ӧǡ����ȫ��
���ˮ���������������Ϊx
H2SO4+2NaOH=Na2SO4+2H2O
98 80
50g��x 8g��10%
![]()
x=1.96%
(2)��ÿ���������ܲ������������Ϊy
H2SO4+Ca��OH��2=CaSO4+2H2O
98 136
1.96%��50t y
![]()
y=1.36t