题目内容
下列物质均为初中化学中常见的物质,其中A、B的组成元素相同,A、B、D、E、F为氧化物,H为改良酸性土壤常用的物质,如图是它们之间的转化关系.请回答: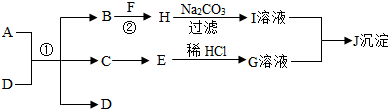
(1)物质D在反应中的作用是 ;
(2)写出反应②的化学方程式:② ;该反应是 反应(选填“放热”或“吸热”)
(3)若J为蓝色沉淀,写出I和G反应生成J的化学方程式 .

(1)物质D在反应中的作用是
(2)写出反应②的化学方程式:②
(3)若J为蓝色沉淀,写出I和G反应生成J的化学方程式
考点:物质的鉴别、推断,物质发生化学变化时的能量变化,书写化学方程式、文字表达式、电离方程式
专题:框图型推断题
分析:根据H为改良酸性土壤常用的物质,所以H是氢氧化钙,氢氧化钙和碳酸钠反应后生成的和碳酸钙沉淀和氢氧化钠,所以I是氢氧化钠,A与D反应后还生成D,可以确定D为催化剂,A与B的元素相同,又有催化剂反应,可以判断该反应是双氧水制取氧气,所以A是过氧化氢溶液,D是二氧化锰,氧化物B和氧化物F会生成氢氧化钙,所以B是水,F是氧化钙,C是氧气,氧气转化成的氧化物E会与盐酸反应,所以E是金属氧化物,然后将推出的各种物质带入转化关系中验证即可.
解答:解:(1)H为改良酸性土壤常用的物质,所以H是氢氧化钙,氢氧化钙和碳酸钠反应后生成的和碳酸钙沉淀和氢氧化钠,所以I是氢氧化钠,A与D反应后还生成D,可以确定D为催化剂,A与B的元素相同,又有催化剂反应,可以判断该反应是双氧水制取氧气,所以A是过氧化氢溶液,D是二氧化锰,氧化物B和氧化物F会生成氢氧化钙,所以B是水,F是氧化钙,C是氧气,氧气转化成的氧化物E会与盐酸反应,所以E是金属氧化物,经过验证,推出的各种物质均满足题中的转化关系,推导正确,所以D是二氧化锰,二氧化锰可以加快过氧化氢的分解速率,而本身的质量和化学性质在反应前后都不会改变,所以二氧化锰在反应中的作用是催化作用;
(2)反应②是氧化钙和水反应生成氢氧化钙,放出大量的热,化学方程式为:CaO+H2O═Ca(OH)2;
(3)若J为蓝色沉淀,所以J是氢氧化铜,G就是氯化铜,E会和盐酸反应生成氯化铜,E是氧化物,可以推出E是氧化铜,氯化铜和氢氧化钠反应生成氢氧化铜沉淀和氯化钠,化学方程式为:2NaOH+CuCl2═Cu(OH)2↓+2NaCl.
故答案为:(1)催化作用;
(2)CaO+H2O═Ca(OH)2,放热;
(3)2NaOH+CuCl2═Cu(OH)2↓+2NaCl.
(2)反应②是氧化钙和水反应生成氢氧化钙,放出大量的热,化学方程式为:CaO+H2O═Ca(OH)2;
(3)若J为蓝色沉淀,所以J是氢氧化铜,G就是氯化铜,E会和盐酸反应生成氯化铜,E是氧化物,可以推出E是氧化铜,氯化铜和氢氧化钠反应生成氢氧化铜沉淀和氯化钠,化学方程式为:2NaOH+CuCl2═Cu(OH)2↓+2NaCl.
故答案为:(1)催化作用;
(2)CaO+H2O═Ca(OH)2,放热;
(3)2NaOH+CuCl2═Cu(OH)2↓+2NaCl.
点评:在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
下列物质的用途中,利用其化学性质的是( )
| A、氧气用于气焊 |
| B、干冰用于人工降雨 |
| C、液氨用作冷冻剂 |
| D、浓硫酸用作于干燥剂 |

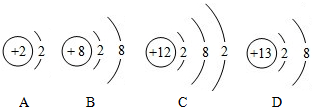 在如图粒子结构示意图中:
在如图粒子结构示意图中: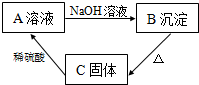 材料:难溶于水的碱在加热的条件下,容易分解生成对应的金属氧化物和水.
材料:难溶于水的碱在加热的条件下,容易分解生成对应的金属氧化物和水.