题目内容
(1)已知点燃条件下5克S与5克O2反应生成10克SO2,则8克硫与16克O2反应后能生成 克SO2.
(2)将20克甲、5克乙、8克丙三种纯净物混合,在密闭容器中加热发生化学反应,经分析可知:反应后混合物中含有5克甲、16克丙,还含有一种新物质丁,则丁物质的质量是 克.
(2)将20克甲、5克乙、8克丙三种纯净物混合,在密闭容器中加热发生化学反应,经分析可知:反应后混合物中含有5克甲、16克丙,还含有一种新物质丁,则丁物质的质量是
分析:(1)已知点燃条件下5克S与5克O2反应生成10克SO2,据此进行分析解答即可.
(2)将20克甲、5克乙、8克丙三种纯净物混合,在密闭容器中加热发生化学反应,经分析可知:反应后混合物中含有5克甲、16克丙,说明参加反应的甲的质量为20g-5g=15g,5克乙全部参加反应,生成的丙的质量为16g-8g=8g;据此由质量守恒定律计算出生成的丁的质量即可.
(2)将20克甲、5克乙、8克丙三种纯净物混合,在密闭容器中加热发生化学反应,经分析可知:反应后混合物中含有5克甲、16克丙,说明参加反应的甲的质量为20g-5g=15g,5克乙全部参加反应,生成的丙的质量为16g-8g=8g;据此由质量守恒定律计算出生成的丁的质量即可.
解答:解:(1)已知点燃条件下5克S与5克O2反应生成10克SO2,则8克硫与8g氧气恰好完全反应后生成16g二氧化硫,氧气有剩余(剩余8g).
(2)将20克甲、5克乙、8克丙三种纯净物混合,在密闭容器中加热发生化学反应,经分析可知:反应后混合物中含有5克甲、16克丙,说明参加反应的甲的质量为20g-5g=15g,5克乙全部参加反应,生成的丙的质量为16g-8g=8g;由质量守恒定律,生成的丁的质量为15g+5g-8g=12g.
故答案为:(1)16 (2)12.
(2)将20克甲、5克乙、8克丙三种纯净物混合,在密闭容器中加热发生化学反应,经分析可知:反应后混合物中含有5克甲、16克丙,说明参加反应的甲的质量为20g-5g=15g,5克乙全部参加反应,生成的丙的质量为16g-8g=8g;由质量守恒定律,生成的丁的质量为15g+5g-8g=12g.
故答案为:(1)16 (2)12.
点评:本题难度不大,掌握质量守恒定律并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
能源和环境问题是世界各国科学家和政府最关注的有关问题,如果不开发新能源,保护环境,人类及其它生命将难以在地球下生存和发展.

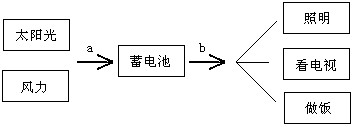
(1)如图是近期央视报道的我国内蒙古地区人们储电、用电方法如下图,试回答:
图中a过程能量转化的形式为:______转化______,使用这种能量的优点是______.
(2)我市城市居民使用燃料主要有天然气、管理煤气(主要成份是CO)和钢瓶装的液化气(主要成份是丁烷C4H10),试回答:
①人们所说的煤气中毒的气体是______.
②查阅资料可知:
| 选项 | 名 称 | 燃 烧 值 | 市场价格 |
| A | 天然气 | 3.9×107J/Kg | 3.5 元/Kg |
| B | 管道煤气 | 1.56×107 J/Kg | 3.7元/Kg |
| C | 液化气 | 4.7×107 J/Kg | 6.0元/Kg |
③如家庭使用正常的天然气因故被告之全市停气,某家庭想用备用的液化气代替天然气,在不改动任何阀门情况下点燃后发现有“火苗不旺”的现象,主要原因是什么?(已知相同条件下,气体体积比等于分子个数比.)