题目内容
【题目】下表是元素周期表中第三周期元素的原子结构示意图。
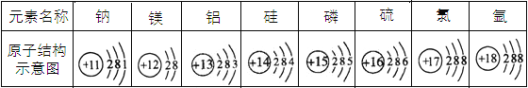
依据上表判断,下列结论正确的是( )
A.11 号元素的原子,在化学反应中容易得到电子变成离子
B.铝元素与硫元素形成化合物的化学式为 Al3S2
C.上述元素称为第三周期元素是因为这些元素的原子核外都有三个电子层
D.Cl→Cl— ,则 Cl 核内有 18 个质子
【答案】C
【解析】
试题分析:A.11 号元素的原子,在化学反应中容易得到电子变成离子是错误的叙述,容易失去电子变为离子;B.铝元素与硫元素形成化合物的化学式为 Al3S2 是错误的叙述,根据化合价的代数和为0,可知化学式为Al2S3 C.上述元素称为第三周期元素是因为这些元素的原子核外都有三个电子层是正确的叙述;D.Cl→Cl— ,则 Cl 核内有 18 个质子是错误的叙述,原子转化为离子时电子改变而质子数不变;故选择C

 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案【题目】某化学兴趣小组通过查阅资料了解到过氧化钠(Na2O2)能与水反应生成氢氧化钠和氧气,于是他们做了以下探究实验。
向盛有过氧化钠粉末的烧杯中加入水,充分反应后,取烧杯中的少量溶液于试管中并加入几滴无色酚酞溶液,溶液变红,过了一会,红色又褪去。
(提出问题)溶液为什么先变红后又褪色了呢?
(交流讨论)甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故。乙同学认为甲同学的猜想不正确,理由是_______。写出氢氧化钠溶液与二氧化碳反应的化学方程式_______。
(查阅资料)①滴加酚酞呈现红色的溶液遇到H2O2时,H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;②酚酞在稀碱性溶液中显红色,而在浓氢氧化钠等浓度较大的碱性溶液中先变红后又褪色。
(作出猜想)
猜想1:酚酞溶液变质
猜想2:过氧化钠与水反应生成了H2O2
猜想3:生成的氢氧化钠溶液浓度太大
(实验探究)同学们设计了下列实验方案进行验证。
实验操作 | 实验现象 | 结论 |
(1)重新配制溶质质量分数为5%的氢氧化钠溶液,向其中滴入几滴无色酚酞溶液 | ____ | 猜想1错误 |
(2)取过氧化钠与水反应后的溶液于试管中,加入适量的二氧化锰后,将带火星的木条放在试管口 | ________ | 猜想2正确 |
(3)取过氧化钠与水反应后的溶液于试管中, ___ | 溶液变红, 一会儿又褪去 | 猜想3错误 |
(拓展延伸)(1)过氧化钠能与二氧化碳反应生成一种白色固体和氧气,该白色固体可能是___。
(2)保存过氧化钠时,应注意____保存。
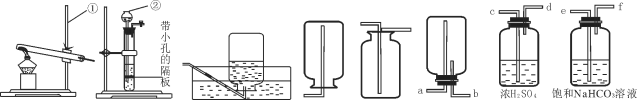
【题目】 (9分) 2011年5月1日,我国实施“醉驾入刑”的新规,引起西园中学化学探究小组的注意,并设计如图实验,对人酒后呼出的气体与空气组成进行比较(不比较水蒸气).

【查阅资料】重铬酸钾溶液与乙醇反应,溶液由黄色变成浅绿色.
【提出假设】
猜想1:呼出的气体中含有乙醇;
猜想2:呼出的气体中 含量比空气的低;
猜想3:呼出的气体中 含量比空气的高.
【实验方案】
(1)按如图装置取气,得空气、呼出气体样品分别于A、C集气瓶中,取多瓶气样备用.
(2)图中澄清石灰水的作用是 .
(3)请填写空格
实验步骤 | 预期现象和结论 |
①向C集气瓶中伸入燃着的木条 | 火焰 ,证明猜想 成立 |
②同时向A、C集气瓶中加入等量的 | 若C集气瓶中 ,且较明显,证明猜想3成立 |
③分别向A、C集气瓶中加入少量重铬酸钾溶液 | 若 ,证明 . |