题目内容
【题目】(1)通常可选用_____检验自来水是硬水还是软水;生活中既能降低水的硬度,又能杀菌消毒的方法是_____;
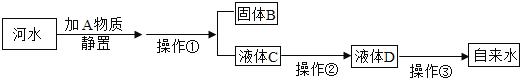
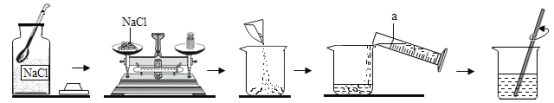
(2)某同学收集到一杯有臭味的浑浊河水,先用滤纸进行过滤,需用到的玻璃仪器有玻璃棒、烧杯和_____;其中玻璃棒的作用是_____;
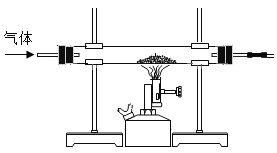
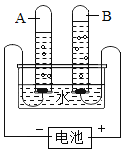
(3)同学们为了探究水的组成,做了电解水实验,如下图所示,写出该实验中反应的文字表达式:_____;该实验证明:_____。
(4)请写出一种生活中的节水方法:_____。
【答案】肥皂水 煮沸 漏斗 引流 ![]() 水是由氢氧两种元素组成 淘米水浇花(合理即可)
水是由氢氧两种元素组成 淘米水浇花(合理即可)
【解析】
(1)常用肥皂水检验硬水还是软水,产生泡沫较多的是软水,泡沫较少的是硬水;生活中既能降低水的硬度,又能杀菌消毒的方法是煮沸;
故答案为:肥皂水;煮沸;
(2)过滤用到的仪器有:铁架台、烧杯、玻璃棒和漏斗;其中玻璃棒的作用是引流;
故答案为:漏斗;引流;
(3)水通电生成氢气和氧气,文字表达式:![]() ,该实验证明了水是由氢氧两种元素组成。
,该实验证明了水是由氢氧两种元素组成。
故填:![]() ;水是由氢氧两种元素组成;
;水是由氢氧两种元素组成;
(4)生活中的节水方法:淘米水浇花,滴灌,及时关紧水龙头等;
故填:淘米水浇花(合理即可)。

 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案【题目】冬天来了,妈妈买了很多暖宝宝回家,小希问妈妈,为什么暖宝宝能发热.妈妈说:听说是里面有铁粉,铁粉生锈放热.为了验证妈妈解释的正确性,小希在实验室打开一片暖宝宝,取出其中黑色粉末做了下面的实验.
I.黑色粉末成分的探究
操作 | 现象 | 结论 |
取暖宝宝中的黑色粉末于试管中,加入足量稀盐酸 | 有气泡冒出, 溶液变为① _____. | 黑色粉末中有铁粉. 产生气泡的方程式②_____. |
反应结束之后,发现仍有固体残留.经过③_____(操作名称),干燥,获得黑色粉末,加热,未能点燃. | —— | —— |
小希查阅资料,发现反应后剩余的黑色粉末可能是活性炭,而活性炭燃烧需要很高的温度,于是小希设计如图 1 的实验.
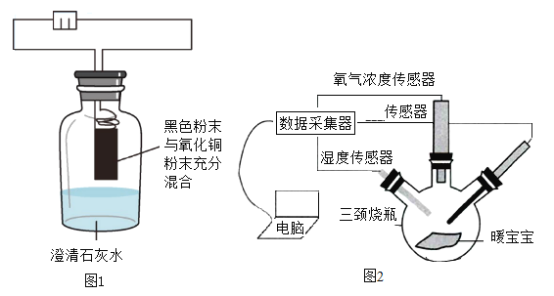
将黑色粉末与氧化铜粉末充分混合,放入加热装置,接通电源,达到高温状态,观察到石灰水变浑浊.小希确定黑色粉末中有活性炭,加热装置中发生的化学反应方程式为④_____.
II.探究“暖宝宝”反应原理现铁的生锈本质是否一致
按图 2(夹持仪器已略去)采用传感器收集数据,将拆除包装的暖宝宝倒入三颈烧瓶中,密封装置,开始收集,观察曲线变化.
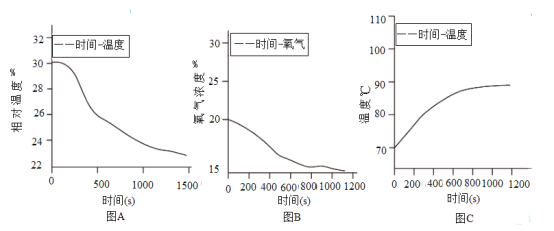
从收集到的图像看暖宝宝发热是因为颗粒微小的铁粉与⑤_____和_____等物质发生反应,并⑥_____热量(填写“吸收”或“放出”).这一反应与铁生锈原理一致.
III.实验拓展
利用上述原理,小希设计使用暖宝宝贴来测定空气中氧气的含量,实验开始前的装置如图 3 所示,
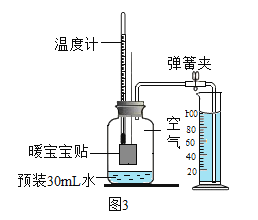
量筒中水的读数为 100mL.
(1)实验过程中,可以观察的现象是⑦_____.
(2)冷却一段时间之后,打开弹簧夹,水从量筒中流入玻璃瓶(容积为 250mL)最后读数为 67mL(铁粉生锈消耗的水忽略不计),通过计算,本实验数据测得空气中氧气的体积分数为⑧_____.
(3)出现上述误差的原因可能是⑨_____(可多选)
A 装置漏气
B 暖宝宝贴中铁粉的使用数量不足
C 温度计的读数未恢复至室温就记录量筒内剩余水的体积
D 弹簧夹未夹紧
E 最后读取量筒中水的体积是俯视读数
【题目】下列图像反应的对应关系正确的是()
|
|
|
|
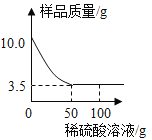
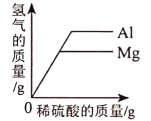
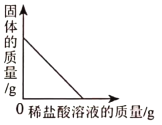
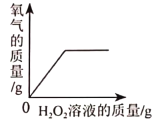
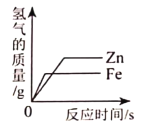
A将足量等浓度的稀硫酸分别滴入等质量的铝粉和镁粉中 | B向一定量的大理石中( 杂质不反应也不溶于水) 加入足量稀盐酸 | C向一定量的MnO2中逐滴加入H2O2溶液 | D相同质量的锌粉和铁粉分别与等浓度的足量稀硫酸反应 |
A.AB.BC.CD.D
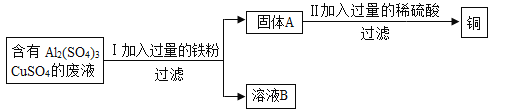
【题目】据统计,我国每年报废的手机超过1亿部,若不进行有效回收利用,会造成巨大的浪费和污染。同学们对废旧手机中的金属回收产生兴趣。

[提出问题]从废旧手机中可以回收到哪些有价值的金属?如何回收?
[查阅资料] I,手机电路板中的金属及其价格如下表所示:
种类 | Fe | Cu | Al | Ni (镍) | Au | Ag | Pd (钯) |
市场价格/ ( $/t) | 365 | 7175.5 | 1710.5 | 14235 | 4.7*107 | 7.6*105 | 2.7*107 |
矿石中含量 | 72.4 | 0.87 | 29.1 | 1.02 | 4 | 120 | 0.4 |
手机电路板中含量 | 5 | 13 | 1 | 0.1 | 350 | 1380 | 210 |
说明: Fe、Cu、 A1、 Ni的含量用质量分数(%)表示,Au、 Ag、 Pd的含量的单位为“g/t”。
II. Ni的金属活动性位于氢前;Pd 的金属活动性位于氢后;NiCl2 溶液为绿色。
Ⅲ.![]()
[实验方案]第一步:选择值得回收的金属。
依据资料I中的数据,废旧手机中有回收价值的金属有Au、Ag、Cu、Pd, 原因是:①它们的市场价格较高;②__________________。
第二步:设计实验分离、回收部分金属。
序号 | 实验步骤 | 实验现象 |
Ⅰ | 取一废旧手机电路板,用电吹风机靠近电路焊接点的焊锡吹热风,一段时间后,用镊子将金属电路从塑料板中拽出 | 焊锡熔化 |
Ⅱ | 将金属电路放入烧杯中,加入过量稀盐酸浸泡 | _______________ |
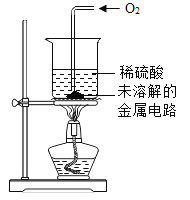
Ⅲ | 取II中未溶解的金属电路,用蒸馏水洗净后,放入如图所示装置中,进行实验。 | 溶液逐渐变成蓝色,仍有微量金属固体未溶解 |
Ⅳ | 过滤Ⅲ中烧杯中的物质,洗涤滤纸上的物质 | 滤纸上仍有微量金属固体 |
Ⅴ | _______________ | _______________ |
[问题讨论]
(1)由步骤I中的现象,可推知的焊锡的物理性质是______________。
(2)步骤II对应的实验现象是______________。
(3)步骤II所得溶液中,一定含有的金属元素是____________。
(4)步骤V的操作是:“向步骤IV获得滤液中加入一定量铁粉”。若该实验过程加入铁粉前后溶液中主要离子变化示意图如图所示。
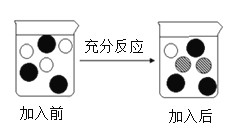
①图中“![]() ”所代表粒子的符号为_______________。
”所代表粒子的符号为_______________。
②充分反应后过滤,滤纸上固体物质是__________________(写化学式); .
③写出该反应的化学方程式_________________。