题目内容
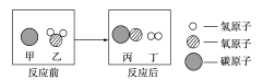
【题目】图1是甲、乙两种物质的溶解度曲线,请结合图2回答问题:

(1)________℃时,甲、乙两种物质的溶解度相等。
(2)溶解度随温度升高而降低的物质是_________(填“甲”或“乙”)。
(3)可使甲物质从其饱和溶液中结晶析出的方法是________________________。
(4)t2℃时,分别将甲、乙两种物质的饱和溶液降温到t1℃,甲溶液的溶质质量分数_______(填“=”、“<”或“>”)乙溶液的溶质质量分数。
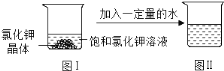
(5)继续用甲物质进行如图2所示的实验:
① 实验过程中,B、C、D对应的溶液为不饱和溶液的是_________。
② 对应的溶液中再加入30g甲固体的过程中,发现固体全部溶解,一段时间后又有部 分固体析出。你认为“全部溶解”的原因是__________________________。
【答案】 t1 乙 降温结晶 > B 甲物质溶解放热,使溶液温度升高,甲物质的溶解度增大
【解析】本题主要考查固体溶解度曲线及其作用;结晶的原理、方法及其应用。在做题时根据溶解度曲线分析:1、溶解度随温度的的变化。2、交点的含义。
(1)t1℃时甲、乙的溶解度曲线交于一点,二者的溶解度相等;
(2)乙的溶解度随温度的升高而降低;
(3)甲的溶解度随温度的升高而增大,可采用降温结晶或冷却热饱和溶液的方法得到晶体;
(4)甲的溶解度随温度升高而增大,乙的溶解度随温度的升高而减小,所以t2℃时,分别将甲、乙两种物质的饱和溶液降温到t1℃,甲析出晶体,依然是饱和溶液,乙变为不饱和溶液,溶质的质量分数与t2℃时相等,观察图示可知:降温后甲在t1℃时的溶解度大于t2℃时乙的溶解度,所以甲溶液的溶质质量分数大于乙溶液的溶质质量分数;
(5)①t1℃时甲的溶解度是65g,所以该温度下50g水中最多溶解32.5g,因此B为不饱和溶液,C中加入了溶质共50g,溶解32.5g,为饱和溶液;升温至t2℃,该温度下甲的溶解度是90g,50g水最多溶解45g溶质,故依然是饱和溶液;
②向B对应的溶液中再加入30g甲固体的过程中,发现固体全部溶解,一段时间后又有部分固体析出,可能是由于甲溶于水放出热量,温度升高溶解度增大,溶解的甲质量就多,温度降下来后溶解度又减小,又会有晶体析出;

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】小刚用pH试纸测得家庭常用洗涤剂的pH如下表所示:
物质 | 厕所清洁剂 | 洗发精 | 洗衣液 | 厨房清洁剂 |
pH | 1 | 8 | 10 | 13 |
在没有除锈剂的情况下,可以用来替代除锈剂的是( )
A. 厕所清洁剂 B. 洗发精 C. 洗衣液 D. 厨房清洁剂
【题目】下表列出了除去物质中所含少量杂质的方法,其中正确的是
选项 | 物质 | 所含杂质 | 除去杂质的方法 |
A | N2 | O2 | 将气体缓缓通过足量的灼热焦炭 |
B | CaO | CaCO3 | 加水溶解、过滤 |
C | Fe | Zn | 加入过量的稀盐酸,过滤,洗涤,干燥 |
D | FeCl2溶液 | CuCl2溶液 | 加入过量的铁粉, 过滤 |
A. A B. B C. C D. D