题目内容
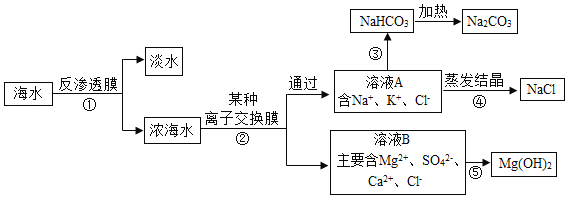
【题目】某工厂排放的工业废水中含有硫酸亚铁和少量硫酸铜。下图是从该废水中回收金属铜和硫酸亚铁晶体的主要流程,请回答下列问题:

(1)工业废水中加入铁粉后发生反应的化学方程式为______________。
(2)操作I名称为______________。
(3)进行操作I前加入稀硫酸的目的是___,能否用稀盐酸代替?_______(填“能”或“不能”),原因是______________。
(4)实验室稀释浓硫酸的具体操作为______________。
【答案】![]() 过滤 除去铜中过量的铁粉 不能 因为这样会生成氯化亚铁使硫酸亚铁不纯净 将浓硫酸酸缓慢沿内壁倒入水中,并不断搅拌
过滤 除去铜中过量的铁粉 不能 因为这样会生成氯化亚铁使硫酸亚铁不纯净 将浓硫酸酸缓慢沿内壁倒入水中,并不断搅拌
【解析】
(1)工业废水中含有硫酸亚铁和少量硫酸铜,按照流程加入铁粉后,铁粉会与硫酸铜生成硫酸亚铁和铜,反应方程式:![]() ;
;
(2)操作一之后形成了固体和溶液,分离固体和溶液的方法是过滤;
(3)因工业废水中加了过量铁粉,因此得到的固体中有铜和过量的铁,加入稀硫酸的目的是为了将铜中的铁粉除去,生成硫酸亚铁,提高硫酸亚铁的回收率;
(4)铁和盐酸反应会生成氯化亚铁,而该流程是为了回收硫酸亚铁晶体,若生成氯化亚铁则会导致硫酸亚铁不纯,故不能用稀盐酸代替稀硫酸;
(5)浓硫酸的稀释需要将浓硫酸酸缓慢沿内壁倒入水中,并不断搅拌防止局部温度过高沸腾;
故答案为:![]() ;过滤;除去铜中过量的铁粉;不能;因为这样会生成氯化亚铁使硫酸亚铁不纯净;将浓硫酸酸缓慢沿内壁倒入水中,并不断搅拌。
;过滤;除去铜中过量的铁粉;不能;因为这样会生成氯化亚铁使硫酸亚铁不纯净;将浓硫酸酸缓慢沿内壁倒入水中,并不断搅拌。

【题目】石灰石高温煅烧获得的生石灰是炼钢生产中的主要碱性造渣材料,其活性度好坏对冶炼过程有重要影响。
(提出问题)哪些因素可能影响生石灰的活性度?
(查阅资料)生石灰活性度体现了生石灰与其他物质的反应能力,是表征生石灰水化反应速度的一个指标。生产中常用的检测标准定义为:在足够时间内,用中和生石灰消化时产生的Ca(OH)2所消耗的盐酸的体积数(单位为mL)表示。
(进行实验)
实验1:相同条件下,煅烧不同石灰石,测生石灰的活性度。
产地 | 石灰石 | 生石灰 | |
外观 | CaO含量/% | 活性度/mL | |
A地 | 灰白色 | 94.89 | 391 |
B地 | 灰白色带少量红棕色 | 89.97 | 375 |
实验2:取某石灰石试样,在电炉内进行煅烧,烧成后测定生石灰的活性度。
时间/min | 各煅烧温度下的生石灰活性度/mL | |||||
1050℃ | 1100℃ | 1150℃ | 1200℃ | 1250℃ | 1300℃ | |
12 | 790 | 836 | 868 | 808 | 454 | 412 |
16 | 793 | 856 | 871 | 845 | 556 | 530 |
20 | 795 | 863 | 873 | 864 | 617 | 623 |
实验3:煅烧温度1050℃时,加NaCl和不加NaCl,比较煅烧石灰石的分解率(分解率影响生石灰活性度)。

(解释与结论)
(1)实验1的目的是___________。
(2)能证明最佳煅烧温度为1100~1200℃的证据是__________。
(3)实验3的结论是_________。
(反思与评价)
(4)写出石灰石高温分解生成生石灰和另一种氧化物的化学方程式_________。
(5)除以上研究的可能影响生石灰活性度的因素外,你认为还可以研究的其他因素有_______(写出一条即可)。