题目内容
 据图回答:
据图回答:
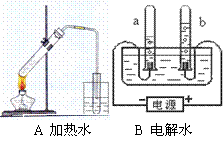
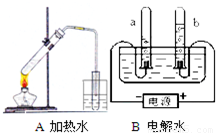
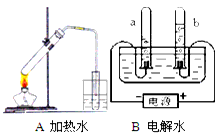
(1)认真观察A、B两装置,写出B装置中发生反应的化学符号表达式________,水中氢元素和氧元素的质量比为________;用分子和原子的观点分析比较A装置和B装置在试验过程中水的变化情况________.
(2)根据水电解的实验回答:①与电源________极(填“正”或“负”)相连的一端产生氢气的体积为100mL时,另一端产生的氧气的体积约为________mL.
②若在此条件下,氢气的密度为0.09g/L,氧气的密度为1.43g/L.则生成的这些氧气的质量为________g,氢气的质量为________g.
③晓露同学在实验时发现生成的氢气与氧气的体积比约大于理论比值.你认为可能的原因是(答一条即可)________.
解:(1)B装置为电解水,水在通电条件下分解成氢气和氧气,反应的化学方程式为H2O 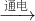 H2+O2;根据水的化学式H2O,水中氢元素和氧元素的质量比=(1×2):16=1:8;
H2+O2;根据水的化学式H2O,水中氢元素和氧元素的质量比=(1×2):16=1:8;
A装置对水加热,水分子间间隔变大,水由液体变成气体,水分子本身并没有发生改变;B装置电解水,水分子变成了氢分子和氧分子,分子本身改变;
(2)①与电源负极相连的一端产生的是氢气,正极产生氧气,且氢气与氧气的体积比为2:1,故氢气体积为100mL时,另一端产生的氧气的体积约为50mL.
②若在此条件下,氢气的密度为0.09g/L,氧气的密度为1.43g/L.则生成的这些氧气的质量为50mL×10-3×1.43g/l=0.0715g;氢气的质量为100mL×0.09g/L=0.009g;
③晓露同学在实验时发现生成的氢气与氧气的体积比约大于理论比值.可能的原因是氧气在水中的溶解能力比氢气大(或产生的氧气会与金属电极发生氧化反应,从而消耗一部分氧气).
故答案为:(1)H2O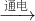 H2+O2;1:8;A中的水分子本身没有改变,改变的是分子之间的间隔;B中的水分子发生了改变,变成了氢气分子和氧气分子;
H2+O2;1:8;A中的水分子本身没有改变,改变的是分子之间的间隔;B中的水分子发生了改变,变成了氢气分子和氧气分子;
(2)①负;50;②0.0715;0.009;
③氧气比氢气更易溶于水或氧气的氧化性很强,与金属电极发生了氧化反应,消耗了一部分氧气.
分析:(1)A装置加热水,可观察到水变成水蒸气,水蒸气遇冷又凝聚成水;B装置电解水,可观察到生成了氢气和氧气,且两气体的体积比为2:1;根据两个实验现象,分析变化中分子、原子的变化,得出实验过程中水分子的变化情况.
(2)可以根据电解水的过程方面进行分析、判断,从而得出正确的结论.
点评:根据物质的化学式,利用元素的相对原子质量与分子中原子个数乘积的比可计算化合物中组成元素的质量比.
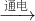 H2+O2;根据水的化学式H2O,水中氢元素和氧元素的质量比=(1×2):16=1:8;
H2+O2;根据水的化学式H2O,水中氢元素和氧元素的质量比=(1×2):16=1:8;A装置对水加热,水分子间间隔变大,水由液体变成气体,水分子本身并没有发生改变;B装置电解水,水分子变成了氢分子和氧分子,分子本身改变;
(2)①与电源负极相连的一端产生的是氢气,正极产生氧气,且氢气与氧气的体积比为2:1,故氢气体积为100mL时,另一端产生的氧气的体积约为50mL.
②若在此条件下,氢气的密度为0.09g/L,氧气的密度为1.43g/L.则生成的这些氧气的质量为50mL×10-3×1.43g/l=0.0715g;氢气的质量为100mL×0.09g/L=0.009g;
③晓露同学在实验时发现生成的氢气与氧气的体积比约大于理论比值.可能的原因是氧气在水中的溶解能力比氢气大(或产生的氧气会与金属电极发生氧化反应,从而消耗一部分氧气).
故答案为:(1)H2O
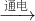 H2+O2;1:8;A中的水分子本身没有改变,改变的是分子之间的间隔;B中的水分子发生了改变,变成了氢气分子和氧气分子;
H2+O2;1:8;A中的水分子本身没有改变,改变的是分子之间的间隔;B中的水分子发生了改变,变成了氢气分子和氧气分子;(2)①负;50;②0.0715;0.009;
③氧气比氢气更易溶于水或氧气的氧化性很强,与金属电极发生了氧化反应,消耗了一部分氧气.
分析:(1)A装置加热水,可观察到水变成水蒸气,水蒸气遇冷又凝聚成水;B装置电解水,可观察到生成了氢气和氧气,且两气体的体积比为2:1;根据两个实验现象,分析变化中分子、原子的变化,得出实验过程中水分子的变化情况.
(2)可以根据电解水的过程方面进行分析、判断,从而得出正确的结论.
点评:根据物质的化学式,利用元素的相对原子质量与分子中原子个数乘积的比可计算化合物中组成元素的质量比.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案
相关题目
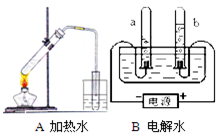 据图回答:
据图回答: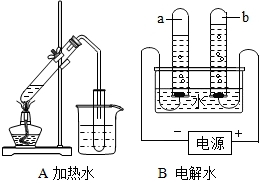 据图回答:(1)认真观察A、B两装置,写出B装置反应的文字表达式
据图回答:(1)认真观察A、B两装置,写出B装置反应的文字表达式 ,水中氢元素和氧元素的质量比为 ;用分子和原子的观点分析比较A装置和B装置在试验过程中水的变化情况 。
,水中氢元素和氧元素的质量比为 ;用分子和原子的观点分析比较A装置和B装置在试验过程中水的变化情况 。