题目内容
氢气和氧气混合气体共15g,点燃充分反应后还剩下氧气1.5g,求原混合气体中氢气和氧气的质量各占多少?
解:设参加反应的氢气为xg,参加氧气的质量为(15-1.5g-x);根据题意得:
2H2+O2 2H2O
2H2O
4 32
xg (15-1.5-x)g
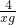 =
=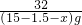
解得:x=1.78g
因为氢气和氧气的混合气体共15g,点燃充分反应后还剩下氧气1.5g,所以混合气体中氢气1.78g,氧气占15g-1.78g=13.22g.
答:原混合气体中氢气的质量为1.78g,氧气的质量为13.22g.
分析:根据题意在分析已知量和未知量之间的质量关系时,要注意找出隐蔽的条件.对于该题已知生成物的质量,根据化学方程式可求出反应物的质量.
点评:在解此类题时,首先根据题中的条件列出关系式,解出题中需要的量,然后结合题意在进一步解答.
2H2+O2
 2H2O
2H2O 4 32
xg (15-1.5-x)g
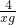 =
=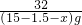
解得:x=1.78g
因为氢气和氧气的混合气体共15g,点燃充分反应后还剩下氧气1.5g,所以混合气体中氢气1.78g,氧气占15g-1.78g=13.22g.
答:原混合气体中氢气的质量为1.78g,氧气的质量为13.22g.
分析:根据题意在分析已知量和未知量之间的质量关系时,要注意找出隐蔽的条件.对于该题已知生成物的质量,根据化学方程式可求出反应物的质量.
点评:在解此类题时,首先根据题中的条件列出关系式,解出题中需要的量,然后结合题意在进一步解答.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目