题目内容
a,b两物质的溶解度曲线如图l所示,请根据图回答: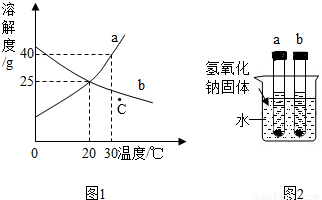
(1)c点配置的a物质溶液降温到0℃时溶液变为 (填“饱和溶液”,“不饱和溶液”).
(2)取30℃时配置的a,b两物质的饱和溶液降温至20℃时,a溶液质量分数 b溶液的质量分数(填“=”,“>”,“<”).
(3)如图2所示,现有20℃时等质量的a、b两物质的饱和溶液,试管底部有等质量的a,b剩余,向烧杯的水中加入氢氧化钠固体,则对相关变化判断正确的 (不考虑溶剂的蒸发,析出的固体不含水)
A、a溶液中溶质质量增多,b溶液中溶质质量减少 B、试管底部a固体的质量大于b固体的质量
C、a溶液中溶剂质量小于b溶液中溶剂质量 D、试管底部a固体的质量小于b固体的质量.
【答案】分析:(1)比较溶解度曲线中点的位置关系,分析温度改变对溶液的影响;
(2)对比两物质溶解度曲线,分析两种物质的饱和溶液在降温时溶液组成的变化,比较所得溶液溶质质量分数的大小;
(3)结合曲线中两物质溶解度曲线的变化,分析升温后饱和溶液中未溶解溶质的质量变化.
解答:解:(1)c点位于a溶解度曲线下方,说明c点的溶液为此温度下a物质的不饱和溶液;当温度降至0℃时,a物质的溶解度随温度降低而减小,且0℃的溶解度低于c点,所以,降温至0℃溶液析出少量晶体后变成饱和溶液;
故答案为:饱和溶液;
(2)30℃时的a,b两物质的饱和溶液,降温时,a物质的饱和溶液析出晶体变成20℃的饱和溶液,溶液的溶质质量分数减小,而b物质的饱和溶液降温变成了不饱和溶液,溶液的组成不变,溶液的溶质质量分数不变;又由溶解度曲线图,20℃时a物质的溶解度位于30℃的b物质溶解度上方,因此,降温到20℃时,两溶液的溶质质量分数大小关系为:a>b;
故答案为:>;
(3)向烧杯中加入氢氧化钠,氢氧化钠溶于水放出大量热而使两物质的饱和溶液温度升高,因a物质溶解度随温度升高而减小,所以有固体析出,则试管底部的固体质量增加;而b物质溶解度随温度升高而增大,试管底部b固体减少;
故选AD.
点评:20℃时两物质的溶解度相等,此时两物质的饱和溶液的溶质的质量分数相等,但由30℃的饱和溶液降温至20℃时,物质b的饱和溶液变成了不饱和溶液,所以,不能再使用上述相等的结论进行判断.
(2)对比两物质溶解度曲线,分析两种物质的饱和溶液在降温时溶液组成的变化,比较所得溶液溶质质量分数的大小;
(3)结合曲线中两物质溶解度曲线的变化,分析升温后饱和溶液中未溶解溶质的质量变化.
解答:解:(1)c点位于a溶解度曲线下方,说明c点的溶液为此温度下a物质的不饱和溶液;当温度降至0℃时,a物质的溶解度随温度降低而减小,且0℃的溶解度低于c点,所以,降温至0℃溶液析出少量晶体后变成饱和溶液;
故答案为:饱和溶液;
(2)30℃时的a,b两物质的饱和溶液,降温时,a物质的饱和溶液析出晶体变成20℃的饱和溶液,溶液的溶质质量分数减小,而b物质的饱和溶液降温变成了不饱和溶液,溶液的组成不变,溶液的溶质质量分数不变;又由溶解度曲线图,20℃时a物质的溶解度位于30℃的b物质溶解度上方,因此,降温到20℃时,两溶液的溶质质量分数大小关系为:a>b;
故答案为:>;
(3)向烧杯中加入氢氧化钠,氢氧化钠溶于水放出大量热而使两物质的饱和溶液温度升高,因a物质溶解度随温度升高而减小,所以有固体析出,则试管底部的固体质量增加;而b物质溶解度随温度升高而增大,试管底部b固体减少;
故选AD.
点评:20℃时两物质的溶解度相等,此时两物质的饱和溶液的溶质的质量分数相等,但由30℃的饱和溶液降温至20℃时,物质b的饱和溶液变成了不饱和溶液,所以,不能再使用上述相等的结论进行判断.

练习册系列答案
相关题目
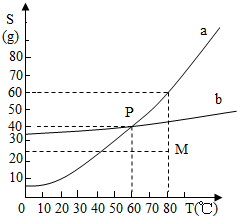 如如图所示为a、b两物质的溶解度曲线,下列根据如图所示中M点和P点,得到的正确信息是( )
如如图所示为a、b两物质的溶解度曲线,下列根据如图所示中M点和P点,得到的正确信息是( )| A、60℃时,a、b两物质饱和溶液的质量分数都为40% | B、80℃时,100g水中溶解25g的a的物质,溶液不饱和 | C、80℃时,将a、b两物质的饱和溶液降温到20℃时,只有a物质析出 | D、向M点的任意量a溶液中,加入(60-25)g溶质,溶液一定达到饱和 |
 25、如图为a、b、c三种物质的溶解度曲线.
25、如图为a、b、c三种物质的溶解度曲线.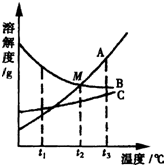 25、A、B、C三种物质的溶解度曲线如右图所示,请回答:
25、A、B、C三种物质的溶解度曲线如右图所示,请回答: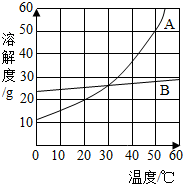 (2012?集美区质检)如图是A、B两种固体物质的溶解度随温度变化的曲线.请回答:
(2012?集美区质检)如图是A、B两种固体物质的溶解度随温度变化的曲线.请回答: