题目内容
已知CaO、CuO、SO2、CO等属于氧化物;NH3、CH4、HF、NaH、KH等属于氢化物.则下列说法中,错误的是( )
A. 氢化物可理解为由两种元素组成,其中一种是氢元素的化合物
B. 水既属于氧化物又属于氢化物
C. 硫酸既属于氧化物又属于氢化物
D. 在NaH中,钠元素显+1价
 名校课堂系列答案
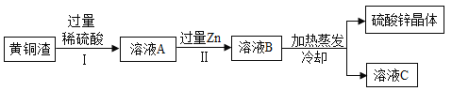
名校课堂系列答案把一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下,下列说法中正确的是( )
物质 | a | b | c | d |
反应前的质量(g) | 6.4 | 3.2 | 2.8 | 4.0 |
反应后的质量(g) | 5.2 | X | 2.8 | 7.6 |
A. a和d是反应物 B. c一定是催化剂
C. X=2.4g D. 该反应是化合反应
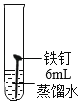
某兴趣小组发现铁钉生锈需要几天的时间,询问老师如何加快铁钉生锈的速度。
老师说氯化物可能加快铁钉生锈的速度。
(提出问题)氯化物对铁钉生锈有怎样的影响?
(查阅资料)
ⅰ.NaCl、CaCl2、CuCl2等由氯离子与金属离子构成的盐属于氯化物。
ⅱ.铜能与氧气反应,生成黑色的CuO。
ⅲ.CuO能与稀硫酸发生反应:CuO+H2SO4═CuSO4+H2O。
(进行实验、分析解释、获得结论)
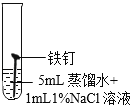
实验1:探究氯化物对铁钉生锈速度的影响。
试管 编号 | ① | ② | ③ | ④ |
实验 |
|
|
|
|
现象 | 2天后,铁钉表面出现红色 | 1天后,铁钉表面出现红色 | 1天后,铁钉表面出现红色 | 7分钟时铁钉表面出现红色,20分钟后试管底部出现红色沉淀 |
(1)对比实验①②③可以得到的结论是___。
(2)小组同学认为,试管④中的红色沉淀可能是铁锈,也可能是铜。他们认为红色沉淀可能是铜的理由是___(用化学方程式解释)。
实验2:探究试管④中红色沉淀的物质组成。
实验步骤 | 实验操作 | 实验现象 |
Ⅰ | 取出试管④中的铁钉,过滤剩余物,洗涤滤纸上的物质 | 固体为红色 |
Ⅱ | 将步骤Ⅰ所得红色固体加入试管中,再向试管中加入足量的 | 红色固体大部分溶解,溶液变为黄色 |
Ⅲ | 将步骤Ⅱ所得混合物过滤,洗涤、干燥滤纸上的固体后,置于石棉网上充分加热 | 红色固体变黑 |
Ⅳ | 向试管中加入步骤Ⅲ所得黑色固体,再加入足量稀硫酸 | 黑色固体全部溶解,溶液变为蓝色 |
(3)步骤Ⅱ中所加入的试剂是___。
(4)步骤Ⅲ、Ⅳ的实验目的是___。
(5)由实验2可得出结论:试管④中红色沉淀的物质组成是___。
(反思与评价)
(6)结合实验1、2的结论,对于“氯化物对铁钉生锈速度的影响”,小组同学提出了进一步的假设:___。


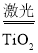 2H2↑+O2↑。二氧化钛中钛元素化合价为_____,分解海水时二氧化钛的作用是_____,生成的氢气用于燃料电池时,实现了_____能转变为电能。
2H2↑+O2↑。二氧化钛中钛元素化合价为_____,分解海水时二氧化钛的作用是_____,生成的氢气用于燃料电池时,实现了_____能转变为电能。