题目内容
【题目】某固体混合物内含有A、B、C三种物质各10g,将其充分反应后,B消耗完全,C的质量增加了8g,生成了4gD,若A全部参加反应,需再加入B的质量是
A.25g B.20g C.40g D.30g
【答案】C
【解析】
试题分析:由题意可知:A+B→C+D,10gB消耗完全时,生成了8gC和4gD,根据质量守恒定律:那么参加反应的A是:8g+4g-10g=2g,A还剩余8g,设需再加入B的质量是x,那么
A+B→C+D
2g 10g
8g x
2克:8克=10克:X
X=40克 故选C

练习册系列答案
相关题目
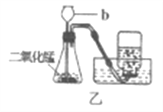
【题目】在实验室中甲乙两位同学分别进行了如下实验,其中甲观察到固体全部消失有气泡冒出,甲同学实验中发生的反应类型是______,乙同学实验中观察到的现象是______。反应结束后甲乙两位同学将仪器中药品全部倒在一个大烧杯中后观察到有气泡冒出和大量白色沉淀生成。

【问题】:反应后大烧杯中上层清液中中含有哪些溶质?
【猜想】:①可能只含有:NaCl ②可能含有CaCl2、NaCl ③可能含有CaCl2、NaCl 和 Na2CO3 ④ 可能含有、NaCl 、Na2CO3 。
甲乙两位同学通过讨论一致认为上述猜想_____ 一定不成立,理由是_________。
【实验】:
实验步骤 | 实验现象 | 实验结论 |
1、取少量上层清液于一支试管中,滴加足量K2CO3溶液 | ___________ | 猜想②不成立 |
2、取少量上层清液于一支试管中,滴加足量Ba(NO3)2溶液 | 白色沉淀 | 猜想________ 成立 |
3、取少量上层清液于一支试管中,滴加1-2滴酚酞 | ___________ |