题目内容
小华测定Cu-Zn合金及Cu-Ag合金中铜的质量分数,实验室只提供一瓶未标明质量分数的稀盐酸和必要的仪器.(1)你认为能测出其铜的质量分数的是
(2)小华取该合金的粉末65g与足量该盐酸充分反应,经测定,产生了0.4g气体,请求出该合金中铜的质量分数.
解:设合金中含铜的质量为x
Zn+2HCl═ZnCl2+H2↑
65 2
65g-x 0.4g
| 65 |
| 2 |
| 65g-x |
| 0.4g |
x=52g
则合金中铜的质量分数为:
| 52g |
| 65g |
答:混合物中含铜的质量分数为80%.
(3)若想测出该盐酸的质量分数,实验时必须提供和测出的数据是
A.参加反应的合金质量;B.参加反应的稀盐酸的质量;C.产生气体的质量.
分析:(1)由题中提供的药品可知本题中要测出的合金中的两种金属必须一种在氢之前,一种在氢之后;(2)根据氢前金属与盐酸的反应求出金属锌和金属铜的质量进而可求出合金中铜的质量分数;
(3)要求出盐酸中溶质的质量分数必须测出或求出溶质和溶液的质量,而溶液的质量需要测出,溶质的质量需要根据生成氢气的质量计算出来.
(3)要求出盐酸中溶质的质量分数必须测出或求出溶质和溶液的质量,而溶液的质量需要测出,溶质的质量需要根据生成氢气的质量计算出来.
解答:解:(1)因Cu-Ag合金中金属铜和银都位于氢之后,都不能和盐酸反应,所以无法利用金属和盐酸的反应测出合金中铜的质量分数,而Cu-Zn合金中锌可以和盐酸反应而铜不会,所以可利用金属和盐酸的反应测出合金中铜的质量分数.故选Cu-Zn.
(2)因Cu-Zn合金中锌可以和盐酸反应而铜不会,所以可利用生成氢气的质量求出合金镇南关铜和锌的质量然后再求出合金中铜的质量分数.
设合金中含铜的质量为x
Zn+2HCl═ZnCl2+H2↑
65 2
65g-x 0.4g
=
x=52g
则合金中铜的质量分数为:
×100%=80%
答:混合物中含铜的质量分数为80%.
(3)要想测出该盐酸的质量分数,必须知道盐酸中溶质的质量和溶液的质量.参加反应的盐酸中溶质的质量可由生成氢气的质量通过化学方程式计算出,然后(溶质的质量÷稀盐酸的质量)×100%即为该盐酸的质量分数;而参加反应的合金的质量是混合物的质量,进行计算时不能直接使用,实验时必须测出参加反应的稀盐酸的质量和生成氢气的质量.故选BC.
(2)因Cu-Zn合金中锌可以和盐酸反应而铜不会,所以可利用生成氢气的质量求出合金镇南关铜和锌的质量然后再求出合金中铜的质量分数.
设合金中含铜的质量为x
Zn+2HCl═ZnCl2+H2↑
65 2
65g-x 0.4g
| 65 |
| 2 |
| 65g-x |
| 0.4g |
x=52g
则合金中铜的质量分数为:
| 52g |
| 65g |
答:混合物中含铜的质量分数为80%.
(3)要想测出该盐酸的质量分数,必须知道盐酸中溶质的质量和溶液的质量.参加反应的盐酸中溶质的质量可由生成氢气的质量通过化学方程式计算出,然后(溶质的质量÷稀盐酸的质量)×100%即为该盐酸的质量分数;而参加反应的合金的质量是混合物的质量,进行计算时不能直接使用,实验时必须测出参加反应的稀盐酸的质量和生成氢气的质量.故选BC.
点评:本题考查金属活动性顺序及其应用,同时考查根据化学方程式的计算,还从不同角度考查学生分析问题的能力.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
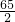 =
=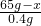
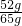 ×100%=80%
×100%=80% =
=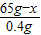
 ×100%=80%
×100%=80%