题目内容
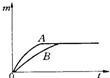 21、用相同质量的铁和锌跟一定量的稀硫酸反应,其反应过程如右图所示(图中横、纵坐标分别表示反应的时间t和产生氢气的质量m).试回答:
21、用相同质量的铁和锌跟一定量的稀硫酸反应,其反应过程如右图所示(图中横、纵坐标分别表示反应的时间t和产生氢气的质量m).试回答:(1)曲线A表示的是
锌
(填:“铁”或“锌”)跟稀硫酸反应的情况.(2)上述曲线图除能说明(1)的结论外,还可以得出另外两个结论,它们是
①产生氢气的质量相等
,②稀硫酸均不足量[或两种金属均过量(足量)(其他合理答案均可)
.分析:“一定量”的稀硫酸,此时稀硫酸可能会出现不足的情况,硫酸的不足会影响到生成氢气的质量;
图中质量相等的两金属停止反应后所得氢气的质量相等,而根据等质量铁和锌与足量酸完全反应铁放出氢气较多,说明金属铁有剩余.
图中质量相等的两金属停止反应后所得氢气的质量相等,而根据等质量铁和锌与足量酸完全反应铁放出氢气较多,说明金属铁有剩余.
解答:解:(1)根据图示,在停止反应前的时间段,相同时间内金属A放出氢气量大于金属B,说明金属A的活动性大于金属B,锌的活动性比铁强,所以金属A为锌;
故答:锌;
(2)图示曲线上待反应停止后,所得氢气质量相等,而相同质量的铁、锌完全反应铁生成氢气量大于锌,所以可以得出铁未完全反应或两种金属均未完全反应的结论;
故答:产生氢气的质量相等;稀硫酸均不足量[或两种金属均过量(足量)(其他合理答案均可).
故答:锌;
(2)图示曲线上待反应停止后,所得氢气质量相等,而相同质量的铁、锌完全反应铁生成氢气量大于锌,所以可以得出铁未完全反应或两种金属均未完全反应的结论;
故答:产生氢气的质量相等;稀硫酸均不足量[或两种金属均过量(足量)(其他合理答案均可).
点评:质量相等的金属与足量酸完全反应,生成氢气质量大小关系可总结为:Al>Mg>Fe>Zn.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
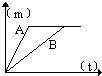 26、用相同质量的铁和锌跟一定量的稀硫酸反应,其反应过程如图所示(横坐标表示反应时间t,纵坐标表示产生H2的质量m).试回答:
26、用相同质量的铁和锌跟一定量的稀硫酸反应,其反应过程如图所示(横坐标表示反应时间t,纵坐标表示产生H2的质量m).试回答: ①曲线A表示的是
①曲线A表示的是
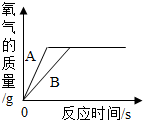 化学兴趣小组同学对“金属活动性顺序”从内容、规律以及应用等方面进行了总结,请按要求填空:
化学兴趣小组同学对“金属活动性顺序”从内容、规律以及应用等方面进行了总结,请按要求填空: (2007?宣武区二模)初中化学课学完以后,化学学习兴趣小组对“金属活动性顺序”从内容、规律以及应用等方面进行了总结.请你认真填写下面的空白内容:
(2007?宣武区二模)初中化学课学完以后,化学学习兴趣小组对“金属活动性顺序”从内容、规律以及应用等方面进行了总结.请你认真填写下面的空白内容: