题目内容
如图是固体硝酸钾的溶解度曲线,根据要求回答下列问题:
(1)硝酸钾溶液中的溶剂是______.
(2)从图溶解度曲线可以得到的信息是______(写一条即可)
(3)欲将一瓶接近饱和的硝酸钾溶液变成饱和溶液,可采取的
方法是______(写出一种即可)
(4)在20℃和50℃两种条件下,某同学对硝酸钾固体进行了如
如图所示的实验,得到相应的溶液①~⑤,其中说法正确的是______.
①
②
③
④
⑤
A.④中溶质的质量分数最大 B.②⑤中溶质的质量分数相等
C.①③④中没有固体存在 D.②④⑤的溶液为饱和溶液.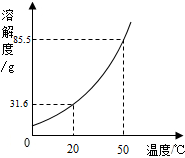
(1)硝酸钾溶液中的溶剂是______.
(2)从图溶解度曲线可以得到的信息是______(写一条即可)
(3)欲将一瓶接近饱和的硝酸钾溶液变成饱和溶液,可采取的
方法是______(写出一种即可)
(4)在20℃和50℃两种条件下,某同学对硝酸钾固体进行了如
如图所示的实验,得到相应的溶液①~⑤,其中说法正确的是______.

| 加入20g |
| KNO3固体 |
| 加入30g |
| KNO3固体 |
| 加热 |
| 至50℃ |
| 加入30g |
| KNO3固体 |
| 降温 |
| KNO3固体 |
A.④中溶质的质量分数最大 B.②⑤中溶质的质量分数相等
C.①③④中没有固体存在 D.②④⑤的溶液为饱和溶液.

(1)硝酸钾溶液中的溶剂是水;
(2)从图溶解度曲线可以得到的信息是:硝酸钾溶解度随温度的升高而增大;
(3)硝酸钾的溶解度随温度的升高而增大,所以将一瓶接近饱和的硝酸钾溶液变成饱和溶液,可采取的方法是降低温度至固体析出(或加入硝酸钾固体等);
(4)由20℃硝酸钾的溶解度为31.6g可知,在20℃100g水中加入20g硝酸钾,硝酸钾全部溶解,形成20℃的不饱和溶液①;再加入30g硝酸钾,只能溶解11.6g,形成20℃的饱和溶液②;升高到50℃,由于50℃硝酸钾的溶解度为85.5g,所以未溶解的硝酸钾全部溶解,但形成的是50℃的不饱和溶液③;再加入30g硝酸钾后,溶质的质量为80g,所以仍然为50℃的不饱和溶液④,但是溶质质量分数比③大;再降温到20℃,又形成20℃的饱和溶液⑤.所以④中溶质的质量分数最大、②⑤中溶质的质量分数相等、①③④中没有固体存在,④为不饱和溶液,故选:ABC.
故答案为:(1)水;(2)硝酸钾溶解度随温度的升高而增大;(3)降低温度至固体析出(或加入硝酸钾固体等);(4)ABC.
(2)从图溶解度曲线可以得到的信息是:硝酸钾溶解度随温度的升高而增大;
(3)硝酸钾的溶解度随温度的升高而增大,所以将一瓶接近饱和的硝酸钾溶液变成饱和溶液,可采取的方法是降低温度至固体析出(或加入硝酸钾固体等);
(4)由20℃硝酸钾的溶解度为31.6g可知,在20℃100g水中加入20g硝酸钾,硝酸钾全部溶解,形成20℃的不饱和溶液①;再加入30g硝酸钾,只能溶解11.6g,形成20℃的饱和溶液②;升高到50℃,由于50℃硝酸钾的溶解度为85.5g,所以未溶解的硝酸钾全部溶解,但形成的是50℃的不饱和溶液③;再加入30g硝酸钾后,溶质的质量为80g,所以仍然为50℃的不饱和溶液④,但是溶质质量分数比③大;再降温到20℃,又形成20℃的饱和溶液⑤.所以④中溶质的质量分数最大、②⑤中溶质的质量分数相等、①③④中没有固体存在,④为不饱和溶液,故选:ABC.
故答案为:(1)水;(2)硝酸钾溶解度随温度的升高而增大;(3)降低温度至固体析出(或加入硝酸钾固体等);(4)ABC.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
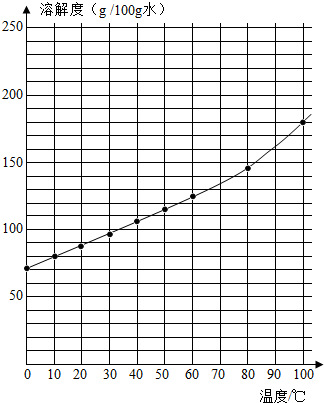
(1)如图是一张绘制到一半的溶解度曲线图,其中只有硝酸钠的溶解度曲线,请根据表格在图中继续画出硝酸钾的溶解度曲线.
 (2)根据溶解度曲线,小李设计了如下实验:
(2)根据溶解度曲线,小李设计了如下实验:
A、B两个烧杯中分别加入10克硝酸钾和硝酸钠,然后分别加入20mL水,在室温(20℃)下,烧杯A中固体全部溶解,烧杯B中尚有固体未溶解.则烧杯A中溶液的质量百分比浓度为 (保留一位小数),烧杯B中所形成的是 (填“悬浊液”、“乳浊液”或“溶液”),如果将烧杯B中不溶的固体过滤之后,剩余溶液是否饱和 (填“是”或“否”);烧杯B中还未溶解的物质为 ,由此可鉴别出硝酸钾和硝酸钠.
| 温度(℃) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 溶解度(g/100g水) | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | 202 | 246 |
 (2)根据溶解度曲线,小李设计了如下实验:
(2)根据溶解度曲线,小李设计了如下实验:A、B两个烧杯中分别加入10克硝酸钾和硝酸钠,然后分别加入20mL水,在室温(20℃)下,烧杯A中固体全部溶解,烧杯B中尚有固体未溶解.则烧杯A中溶液的质量百分比浓度为
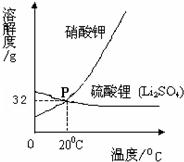
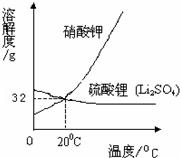 21、21、如图是硝酸钾、硫酸锂二种物质的溶解度曲线图,看图后填空:
21、21、如图是硝酸钾、硫酸锂二种物质的溶解度曲线图,看图后填空: (2007?哈尔滨)如图是同学们根据所学知识设计的一个趣味实验,请参与实验并回答问题:
(2007?哈尔滨)如图是同学们根据所学知识设计的一个趣味实验,请参与实验并回答问题: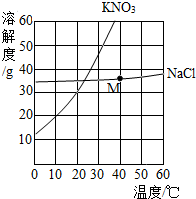 如图是氯化钠、硝酸钾两种固体物质的溶解度曲线.
如图是氯化钠、硝酸钾两种固体物质的溶解度曲线.