题目内容
【题目】(9分)空气、水、金属等是重要的资源。
(1)工业上常把煤块粉碎后使其充分燃烧,其原理是 。
家中堆放杂物的纸箱着火时,可用水浇灭,其原理是 。
(2)铜制品在空气中会发生锈蚀[铜锈的主要成分是Cu2(OH)2CO3]。
①根据铜锈的主要成分中含有氢元素,可以判断出铜生锈需要空气中的 ;根据铜锈的主要成分中含有碳元素,可以判断出铜生锈需要空气中的 。
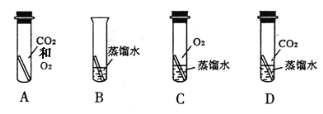
②某化学兴趣小组欲通过实验探究“铜生锈是否需要空气中的氧气?”下图所示实验中(试管内的“![]() ”均为铜片),只需完成实验 和 即可达到探究目的(填字母)。
”均为铜片),只需完成实验 和 即可达到探究目的(填字母)。
(3)铝是世界上年产量第二的金属。
①用坩埚钳夹住一小块铝箔,在酒精灯上加热至熔化,轻轻晃动,观察到熔化的铝被一层膜兜着并不滴落,产生该现象的原因是 。
②铝和氢氧化钠溶液反应的化学方程式为2Al+2NaOH+2X 2NaAlO2+3H2↑,其中X的化学式为 。足量的稀盐酸与氢氧化钠溶液分别和等质量的铝粉充分反应,产生氢气的质量分别为m1、m2,下列有关m1、m2大小关系的说法正确的是 (填字母)。
A.m1>m2 B.m1<m2 C.m1=m2 D.无法比较
【答案】(1)增大燃料与空气的接触面 水可以吸收可燃物燃烧释放出的大量热,使可燃物的温度降到其着火点以下
(2)①H2O CO2 ②B D
(3)①表面氧化铝的熔点高于铝的熔点 ②H2O C
【解析】
试题分析:(1)工业上常把煤块粉碎后使其充分燃烧,其原理是:增大燃料与空气的接触面;根据灭火的原理:(1)消除可燃物(2)隔绝氧气(或空气)(3)降温到着火点以下;家中堆放杂物的纸箱着火时,可用水浇灭,其原理是:水可以吸收可燃物燃烧释放出的大量热,使可燃物的温度降到其着火点以下
(2)①根据铜锈的主要成分中含有氢元素,结合质量守恒定律,可以判断出铜生锈需要空气中的H2O;根据铜锈的主要成分中含有碳元素,可以判断出铜生锈需要空气中的CO2
②化学兴趣小组欲通过实验探究“铜生锈是否需要空气中的氧气,就要注意控制变量,设计对比实验,故只需完成实验B和D即可达到探究目的,因为这两个实验的变量就是一个有氧气,两一个没有氧气
(3)①用坩埚钳夹住一小块铝箔,在酒精灯上加热至熔化,轻轻晃动,观察到熔化的铝被一层膜兜着并不滴落,产生该现象的原因是:表面氧化铝的熔点高于铝的熔点
②根据质量守恒定律的微观解释:在化学反应前后,原子的种类、数目都不变,结合化学反应:2Al+2NaOH+2X 2NaAlO2+3H2↑,可以推出X化学式为H2O;根据化学反应方程式:2Al+2NaOH+2H2O 2NaAlO2+3H2↑中Al与H2的质量关系为9:1,而根据铝和稀盐酸反应的方程式:2Al +6HCl ===2AlCl3+ 3H2↑中Al与H2的质量关系也为9:1,故等质量的铝粉产生氢气的质量分别为m1=m2 ,故选C

 初中学业考试导与练系列答案
初中学业考试导与练系列答案