题目内容
【题目】太阳能光伏发电最关键的材料是高纯硅.三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法.生产流程示意图如下:
![]()
(1)按物质的分类标准,三氯甲硅烷(SiHCl3)是_____(填化合物或混合物).
(2)“精馏”也是蒸馏的一种形式.通过蒸馏可把液体混合物分离开,原理是利用混合物各成分的_____(填“熔点”或“沸点”)不同.
(3)写出SiHCl3(粗)和氢气反应生成高纯硅和氯化氢气体的反应方程式:_____.
(4)为了达到绿色化学和资源综合利用的目的,上述生产流程中某些物质可循环使用,这些物质是_____(填化学式).
(5)整个制备过程必须达到无水无氧。在H2还原SiHCl3过程中若混入O2,可能引起的后果是_____。
【答案】化合物 沸点 SiHCl3+H2![]() Si+3HCl H2、HCl 发生爆炸
Si+3HCl H2、HCl 发生爆炸
【解析】
(1)三氯甲硅烷中各元素按照一定的质量比组成在一起,所以三氯甲硅烷属于化合物,故填化合物;
(2)蒸馏是通过将各成分加热形成气体后再进行分离,利用的是各成分的沸点不同,故填沸点。
(3)三氯甲硅烷与氢气在温度为1084℃时反应生成氯化氢气体,故反应的化学方程式写为:SiHCl3+H2![]() Si+3HCl。
Si+3HCl。
(4)粗硅与氯化氢气体反应生成三氯甲硅烷和氢气,三氯甲硅烷和氢气反应生成高纯硅和氯化氢气体,两个反应中生成的氢气与氯化氢气体均可以循环使用,故填H2、HCl。
(5)在H2还原SiHCl3过程中若混入O2,高温条件下,氢气与氧气的混合气体会急剧燃烧引起爆炸,故填发生爆炸。

 天天练口算系列答案
天天练口算系列答案【题目】(科学探究)在一次实践活动中,化学兴趣小组的同学在实验室利用稀硫酸、Ba(NO3)2溶液、Na2CO3溶液、NaOH溶液模拟化工厂工业废水的处理过程。
(活动一)将四种溶液两两混合判断能否发生反应。
(1)四种溶液中能彼此发生反应的有_____组,写出其中一个反应的化学方程式:_____。
(2)能发生反应但没有明显现象的一组物质反应的微观本质是_____。
(3)实验完毕,同学们将废液倒入同一个大烧杯中,静置,观察,杯底有白色沉淀,上层溶液为无色。并对白色沉淀和上层无色溶液的成分进行了进一步的探究。
(活动二)探究白色沉淀的成分
(进行猜想)猜想①:白色沉淀是Ba2SO4:猜想②:白色沉淀是BaSO4和BaCO3的混合物。
(实验验证)
实验步骤 | 现象 | 结论 |
取少量白色固体于试管中,向其中加入适量的稀硝酸 | _____ | 猜想②正确 |
(活动三)探究废液杯中无色溶液的成分。
①质疑1:小强认为在反应物中有酸,反应的生成物中也有酸,所以无色溶液中就一定含有酸。但小红提出了不同的观点,她认为_____。同学们一致同意小红的观点。
②检验溶液的酸碱度:所用实验用品有_____,经测定溶液的pH>7,呈碱性。
③(如图)
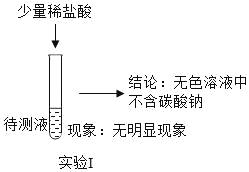
质疑Ⅱ:小林认为实验1不能证明无色溶液中不含碳酸钠,理由是_____,要证明溶液中不含有碳酸钠的实验方案是_____。
得出结论:无色溶液中一定含有的溶质是_____(填化学式)。
(反思与交流)工厂排放出的废液常呈酸性或碱性,排放前我们必须进行处理。