题目内容
金属材料在人类活动中已得到越来越广泛的应用.正确使用金属材料,首先应该了解金属.
(1)①地壳中含量最多的金属元素是________.(填元素符号)
②保持铁的化学性质的最小粒子是________.
(2)国家大剧院安装了近2万块被称作“太空金属”的钛(Ti)金属板,其密度只有钢的60%.钛与稀硫酸反应的化学方程式为:Ti+2H2SO4═Ti(SO4)2+2H2↑.
在某稀有气体中,熔融状态下,镁与TiCl4反应的化学方程式为:TiCl4+2Mg 2MgCl2+Ti.则Mg、Ti、Cu的金属活动性顺序是________.
2MgCl2+Ti.则Mg、Ti、Cu的金属活动性顺序是________.
(3)某实验室废液缸里的废液含有CuSO4、ZnSO4、FeSO4,如果将废液直接排放就会造成水污染.几位同学利用课余处理废液,回收硫酸锌和有关金属.实验过程如下:
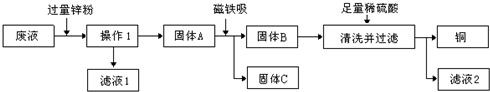
请回答:
①操作1是________,固体A的成分________.
②固体C是________.滤液1和滤液2中溶质相同,该溶质是________.
③写出加入过量锌粉的其中一个反应的化学方程式________;
④加入足量稀硫酸发生反应的化学方程式________.
解:(1)地壳中含量最多的金属元素是铝,金属有原子构成,保持其化学性质的粒子是原子,所以本题答案为:铝,铁原子;
(2)钛与稀硫酸能生成氢气,说明钛在氢前,镁能与TiCl4反应,说明镁在钛的前面,所以本题答案为:Mg>Ti>Cu;
(3)①操作1得到了固体和液体,说明是过滤操作,废液含有CuSO4、ZnSO4、FeSO4,加入过量的锌粉,则锌能将铜和铁置换出来还有剩余,剩余固体A中含有锌、铜和铁,所以本题答案为:过滤,Cu、Zn、Fe;
②铁能被磁铁吸引,而锌和铜不可以,得到的固体B加硫酸能得到铜,故B中含有锌和铜,而C中含有的是铁,锌能与硫酸反应生成硫酸锌,所以本题答案为:Fe,ZnSO4;
③加入过量锌粉能与硫酸铜反应生成硫酸锌和铜,能与硫酸亚铁反应生成铁和硫酸锌,所以本题答案为:
Zn+CuSO4=ZnSO4+Cu;
④加入足量稀硫酸时能与锌反应生成硫酸锌和氢气,所以本题答案为:Zn+H2SO4=ZnSO4+H2↑.
分析:地壳中元素含量前五位的是氧硅铝铁钙,金属是由原子构成的物质,在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
点评:本题考查了金属的有关性质,完成此题,可以依据已有的知识进行,同学们要会利用金属活动顺序表,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.
(2)钛与稀硫酸能生成氢气,说明钛在氢前,镁能与TiCl4反应,说明镁在钛的前面,所以本题答案为:Mg>Ti>Cu;
(3)①操作1得到了固体和液体,说明是过滤操作,废液含有CuSO4、ZnSO4、FeSO4,加入过量的锌粉,则锌能将铜和铁置换出来还有剩余,剩余固体A中含有锌、铜和铁,所以本题答案为:过滤,Cu、Zn、Fe;
②铁能被磁铁吸引,而锌和铜不可以,得到的固体B加硫酸能得到铜,故B中含有锌和铜,而C中含有的是铁,锌能与硫酸反应生成硫酸锌,所以本题答案为:Fe,ZnSO4;
③加入过量锌粉能与硫酸铜反应生成硫酸锌和铜,能与硫酸亚铁反应生成铁和硫酸锌,所以本题答案为:
Zn+CuSO4=ZnSO4+Cu;
④加入足量稀硫酸时能与锌反应生成硫酸锌和氢气,所以本题答案为:Zn+H2SO4=ZnSO4+H2↑.
分析:地壳中元素含量前五位的是氧硅铝铁钙,金属是由原子构成的物质,在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
点评:本题考查了金属的有关性质,完成此题,可以依据已有的知识进行,同学们要会利用金属活动顺序表,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
